Foliar condensate absorption capacity of four typical plant species and their physiological responses to water in the Mu Us Sandy Land of northwestern China
-
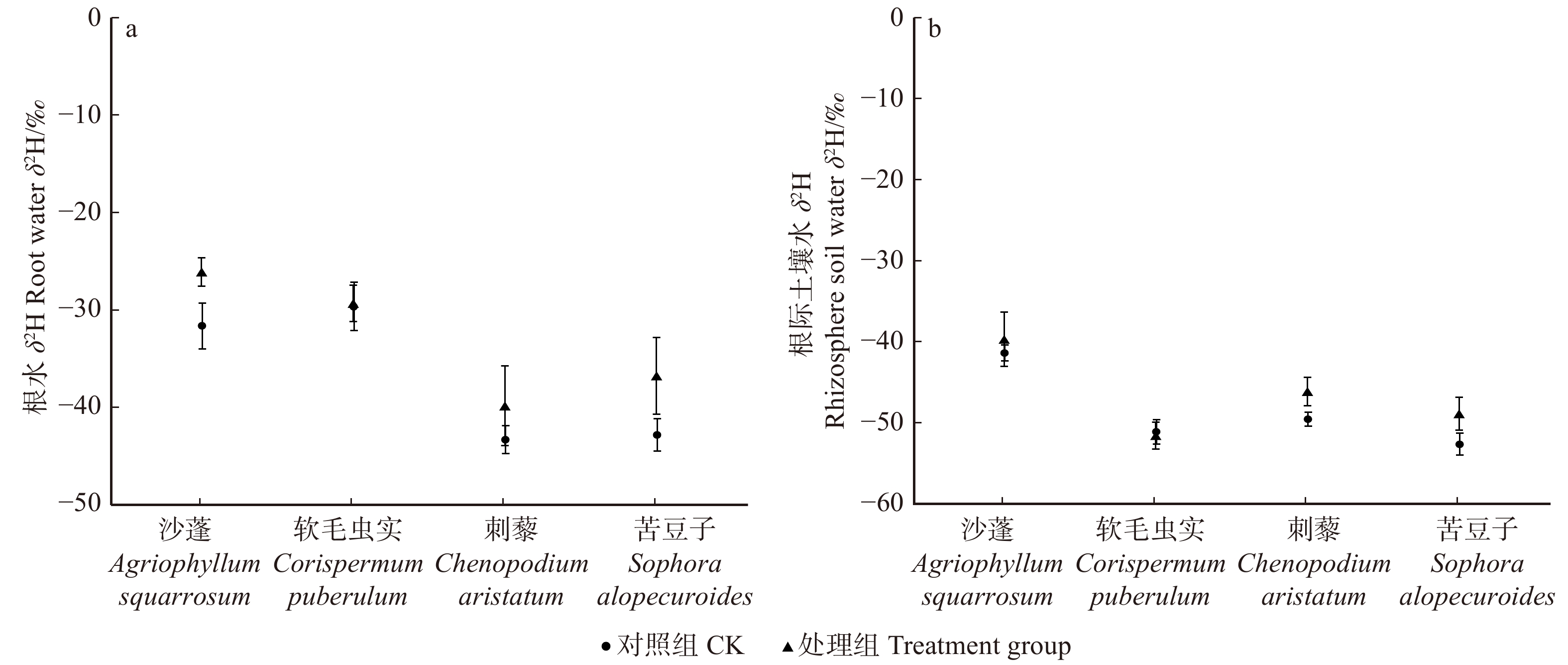
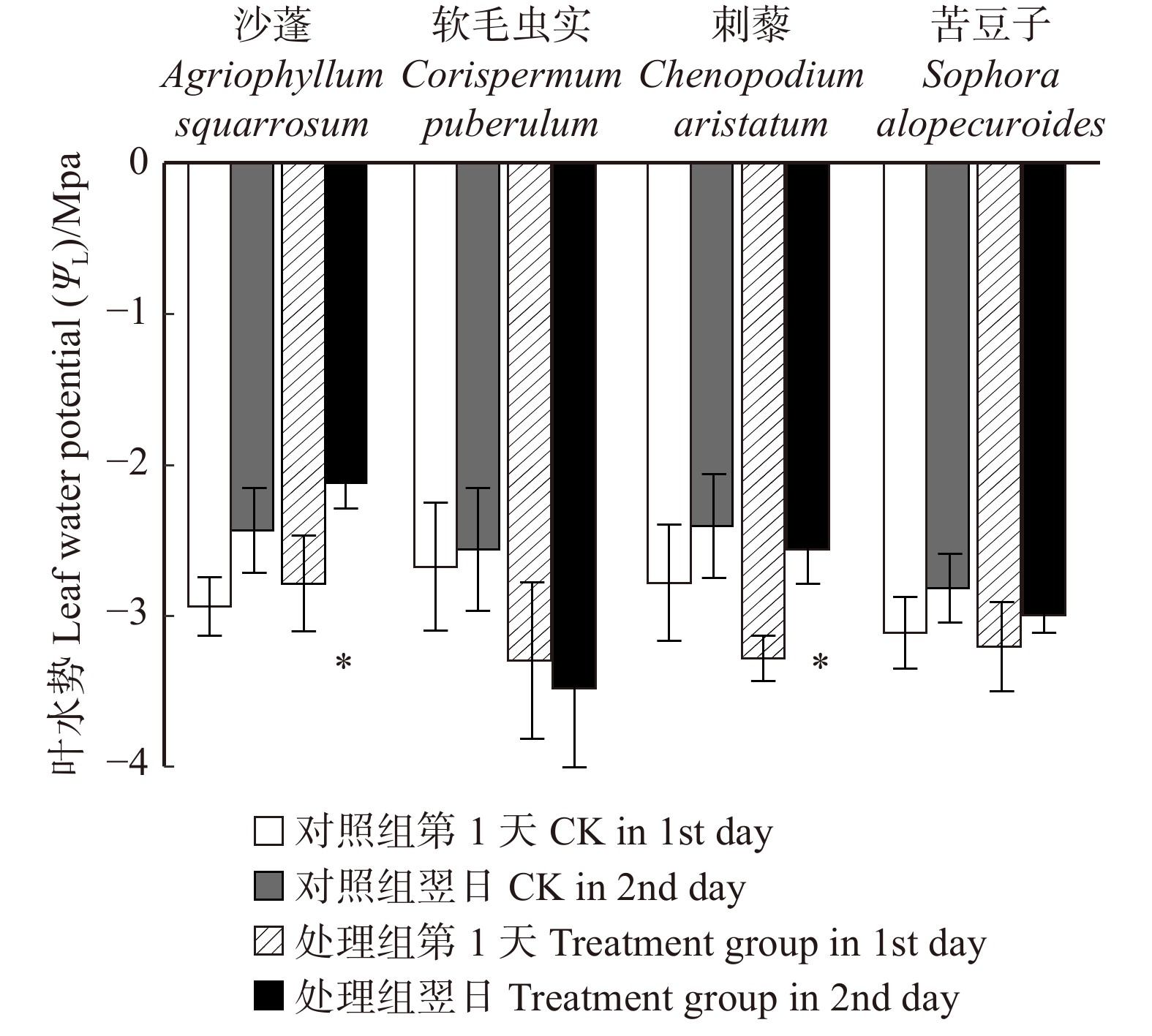
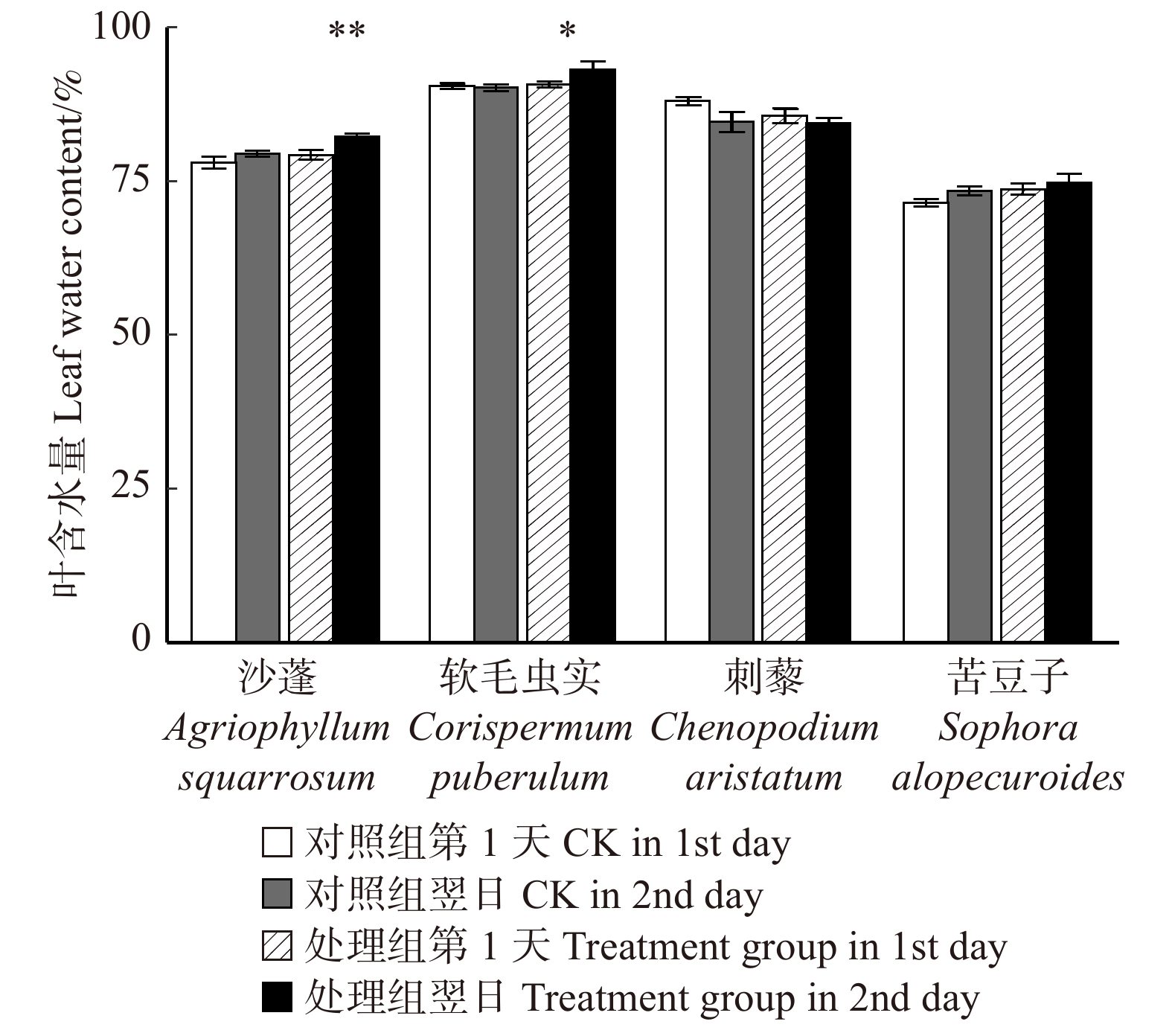
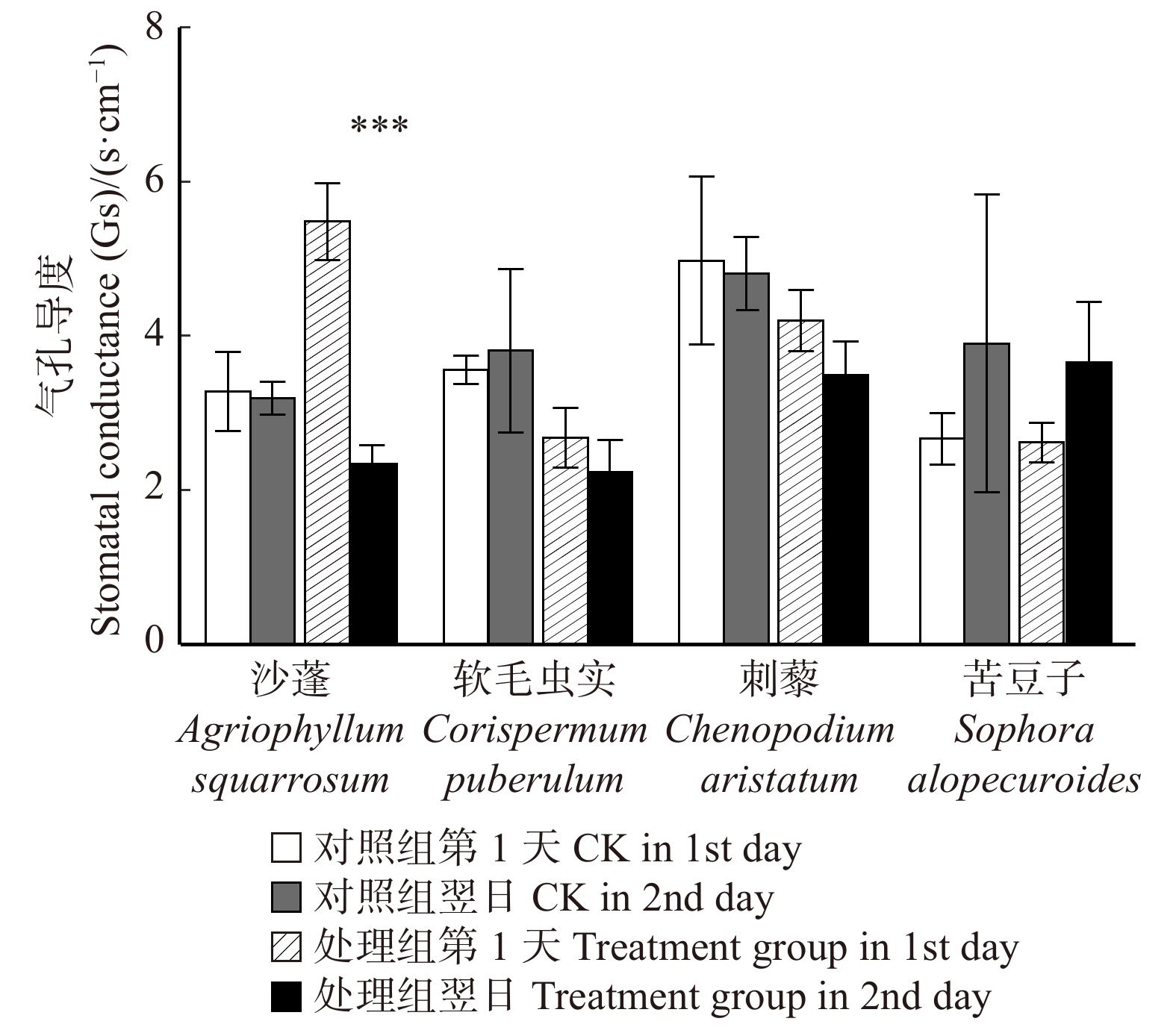
摘要:目的 明确毛乌素沙地4种典型植物沙蓬、软毛虫实、刺藜和苦豆子的叶片凝结水吸收能力,阐明植物叶片对凝结水浸润的水分生理响应。方法 将受试植物置于用高丰度氘水配置的人工标记凝结水环境中,进行凝结水浸润处理,通过比较处理组和对照组植物叶水、根水及根际土壤水的稳定氢同位素丰度变化,确定受试植物叶片是否具有吸水能力,示踪叶片吸收凝结水后,是否将水分转移到植物根系及根际土壤之中;使用露点水势仪、电子天平及气孔计,测定受试植物处理前后的叶水势、叶片含水量和气孔导度变化,了解受试植物对凝结水浸润的水分生理响应。结果 (1)高丰度氘标记凝结水浸润后,处理组4种受试植物的叶水δ2H(20‰ ~ 100‰)均显著高于对照组(−25‰ ~ −15‰),而根水(−45‰ ~ −30‰)及根际土壤水(−50‰ ~ −40‰)则与对照组无显著差异;(2)经过凝结水浸润试验处理,沙蓬的叶水势升高23.81%,叶含水量升高2.94%,气孔导度降低57.40%;软毛虫实的叶含水量升高了2.45%,叶水势和气孔导度无显著变化;刺藜的叶水势升高了21.95%,气孔导度和叶含水量无显著变化;苦豆子的叶水势、叶含水量和气孔导度均无显著变化。结论 毛乌素沙地4种典型植物叶片均具有凝结水吸收能力,叶片吸收的水分未被发现转移至根部或根际土壤。沙蓬、软毛虫实、刺藜通过叶片吸水显著改善了自身水分生理状态,这可能是其适应沙地严酷水分条件的重要水分利用机制,有助于植物存活,而苦豆子叶片对凝结水浸润无明显响应,不能有效利用叶片吸水改变其水分生理状态。Abstract:Objective In this study, we examined Agriophyllum squarrosum, Corispermum puberulum, Chenopodium aristatum, and Sophora alopecuroides in the Mu Us Desert of northwestern China to explore the ability of leaf condensate absorption and their physiological responses to water.Method We determined whether the condensate can be absorbed by the leaves of four plant species, and whether the absorbed water can be transported to the root and rhizosphere soil by dew covered experiments and stable isotope tracer technology to contrast the δ2H values of samples in the leaves, roots and rhizosphere soil from the treatment and control. Meanwhile, we measured leaf water potential (ΨL), leaf water content (wL), and stomatal conductance (Gs) before and after dew treatment by dew point water potential meter, electronic balance and plant porometer in order to evaluate the effects of foliar condensate absorption on the species.Result (1) After the deuterium labelled condensate treatment, the δ2H values in samples of leaves (20‰−100‰) in the treatment group of four plant species were significantly higher than control (−25‰− −15‰); the δ2H values in samples of root(−45‰ − −30‰) and rhizosphere soil (−50‰ − −40‰) in the treatment group did not change significantly compared with control. (2) After the dew treatment, ΨL, wL of A. squarrosum increased by 23.81%, 2.49%, and Gs of it decreased by 57.40%, respectively; wL of C. puberulum increased by 2.45%, but the ΨL and Gs were not change significantly; ΨL of C. aristatum increased by 21.95%, but the wLand Gs were not change obviously; for S. alopecuroides, there were no significant differences in ΨL, wL and Gs.Conclusion We find that all of the four plant species can absorb condensate through leaves, but the water cannot be transported to the root and rhizosphere soil. Agriophyllum squarrosum, Corispermum puberulum and Chenopodium aristatum could improve their water physiological state through water absorption. It may be an important water use strategy for them to adapt to drought environment, for this helps the plants to survive. However, Sophora alopecuroides does not significantly respond to foliar condensate absorption and also could not improve its water physiological state through this process.
-
Keywords:
- condensate /
- foliar water absorption /
- physiological response /
- water use strategy /
- desert plant
-
近年来,以全球变暖为主要标志的气候变化给生态系统带来了巨大的压力[1-4],陆地生态系统的生产力以及水分利用也受到了严重的影响[5-7]。而树木水分利用效率(water use efficiency,WUE)可以反映生态系统对全球气候变化的响应和描述不同生态系统的碳水循环关系 [8]。因此研究WUE不仅可以揭示生态系统对气候变化响应机理,还可以为区域气候变化对生态系统碳水耦合关系的影响提供科学的评价依据。
因研究目的、对象不同,WUE一般可分为生态系统、群体、叶片、以及个体4个方面。生态系统WUE是指植物消耗单位质量水分所固定的二氧化碳或生产干物质的量,因研究尺度、研究领域及获取数据手段的差异,不同的研究对生态系统WUE的计算往往存在一定的区别[9]。群体水平WUE是植物累计一段时期的干物质积累量与作物耗水量的比值,在植物群体水平上研究WUE时,其测算需要在大田试验中进行,工作复杂繁琐,计算出来的WUE不够准确[10]。叶片尺度上的WUE定义为单位通过蒸腾作用消耗单位水量时光合作用形成的有机物量[11],在叶片尺度上研究植物的WUE,只能测得叶片尺度瞬时值,缺乏长时间尺度WUE的研究。而基于树木年轮稳定碳同位素的水分利用效率研究可以反映植物个体的长期WUE[12],已有研究表明这一方法的可行性 [13-15],并且该方法采样破坏性小,测定简单且不受时间和季节的限制[16]。目前国内外学者也进行了许多关于树木年轮稳定碳同位素方法研究植物WUE对气候变化响应的工作,如路伟伟等[17]研究北京山区油松(Pinus tabuliformis)WUE发现,区域整体WUE年际变化与温度呈显著负相关关系,与降水量呈正相关关系。Kannenberg等[18]研究美国西部灌木丛和森林的WUE发现,随着气候变得越来越干燥,美国西南部植物的WUE快速增加。Gagen等[19]利用树轮δ13C研究北芬诺斯干地亚植物的WUE发现,樟子松(Pinus sylvestris)WUE随着CO2浓度的升高而升高,但随着CO2浓度逐渐升高,樟子松WUE的升高出现了阈值。由于生态系统植被类型的多样性以及水分利用的有效性,气候因子对不同生态系统WUE的影响存在较大的差距,不同生态系统WUE的变化特征以及对气候变化的响应也不同。为此针对不同区域生态系统树木WUE进行研究是非常有必要的。
日本柳杉(Cryptomeria japonica)是庐山植被类型的重要树种组成部分,主要分布在海拔700 m以上的常绿针叶人工林,在水源涵养、净化大气环境、森林游憩等生态功能上发挥了重要的作用[20],并且有着较高的生态效益和经济效益。因此本文以庐山日本柳杉作为研究对象,基于树木年轮和稳定碳同位素方法,分析气候变化背景下庐山日本柳杉WUE的变化特征以及庐山日本柳杉WUE与主要气候因子之间的关系,有助于庐山日本柳杉的碳汇能力评估以及提升森林的经营管理水平,对评估庐山日本柳杉的碳水耦合关系提供科学的理论支持。
1. 研究方法与数据来源
1.1 研究区概况
庐山位于江西省九江市(115°51′ ~ 116°07′E,29°30′ ~ 29°41′N),东偎鄱阳湖,海拔25.0 ~ 1 473.8 m,是著名的避暑胜地,气温适度,年平均最高温度32 ℃,最低气温−16.8 ℃,全年平均温11.4 ℃,全年平均降雨量1 917 mm,属湿润气候区(图1)。充足的水热条件及海拔的差异,共同造就了庐山丰富的植被资源[21]。高达40种植物在庐山地区首次被发现或者以庐山(牯岭)来命名。在植被类型区域划分上虽然属于亚热带常绿阔叶林,由于海拔高度具有较大的差异,因此植被类型上又极具多样性。海拔在1 000 m以下多为常绿或者是常绿落叶混交林,海拔在1 000 ~ 1 300 m为落叶阔叶林带[22]。生长在海拔较低处的植被由于受到人为活动的影响,植被破坏较为严重,而海拔较高处植被生长相对较好,对生态系统水源涵养的调节具有一定的作用[23]。
1.2 树木年轮的采集与碳同位素的测定
本研究根据国际树木年轮数据库的采样准则[24],于2019年7月份在庐山3个不同海拔点取样(采样点1、2、3,见图1),海拔分别为800、950和1 150 m,平均树高为18.6、20.0和19.5 m,平均胸径为29.2、30.5和30.1 cm,林分密度为780 株/hm 2,郁闭度 0.6。每个样点取40个样芯。3个采样点的庐山日本柳杉生长良好,受人类活动以及自然灾害影响较小。
通过对日本柳杉样品进行交叉定年[25],选取其树轮无生长异常、年轮宽度变化趋势较为一致、早晚材年轮界限明显的树芯用于稳定同位素的δ13C测定。具体步骤:用不锈钢刀由外而内逐年剥取全木,某些极窄年份的剥取在显微镜的辅助下进行精确切割,将不同树芯的相同年份合并在一起,置于80 ℃的烘箱中烘干至恒质量,枝剪剪碎之后的木材碎屑用高通量组织研磨仪研磨粉碎,过100目筛后装于5 mL离心管中,用于碳同位素测定分析,然后将样品粉末置于V(苯)∶V(乙醇) = 2∶1混合溶液中抽提24 h,除去树脂、树蜡及单宁类等有机物[26]。天平(精度0.001 mg)称取(0.20 ± 0.05) mg抽提好的样品包裹于锡杯中,在赛默飞稳定同位素质谱仪(delta v advantange)中将样品高温燃烧转换为气体,测量精度0.01‰,试验误差小于0.2‰[27],测得稳定碳同位素的比值,即13C丰度(δ13C),每测定10个样品插入1个标样来测定仪器的稳定性(处理的树轮样品在江西农业大学森林培育重点实验室内进行分析测定),根据国际标准进行校正后得到日本柳杉稳定碳同位素δ13C值。
1.3 数据来源及处理
本文所用的气象数据来源于中国气象数据网(http://data.cma.cn/site/index.html)的庐山站日气象数据(庐山站的位置见图1),主要包括1968—2018年的平均气温(T)、最高温度、最低温度、相对湿度、降水量(W)、日照时数、平均风速(Ws)等日值数据。
参考1998年联合国粮农组织推荐的计算公式,利用日照时数数据作为输入参数计算庐山多年的太阳辐射(Rs),详细计算步骤可具体参阅文献[28]。为更准确量化庐山干旱严重程度,使用标准化降水蒸散指数(standardized precipitation evapotranspiration index,SPEI)、标准化降水指数(standardized precipitation index,SPI)以及湿度指数(wet index,WI)来表示庐山地区的干旱情况。SPEI和SPI的计算步骤具体参阅文献[29],WI的计算计算步骤具体参阅文献[30]。利用树木年轮稳定碳同位素值、大气CO2中碳同位素比值和WUE关系来估算庐山日本柳杉1969—2018年的水分利用效率变化,根据Farquhar[13]推荐的公式计算δ13C。
δ13C=(13C/12C)sample−(13C/12C)PDB(13C/12C)PDB×1000‰ (1) 式中:(13C/12C)sample是测试样品13C/12C的摩尔比率; (13C/12C)PDB是标样13C/12C的摩尔比率,δ13C是树木年轮稳定碳同位素比值。
WUE可通过Δ与Ca值之间的关系计算获得[31]。
Δ=δ13Cp−δ13C1+δ13Cp (2) WUE=Ca×(b−Δ)1.6×(b−a) (3) 式中:δ13Cp是大气CO2碳同位素比值,Δ是指树木叶片和空气在光合作用期间同位素水平的差异δ13C的判别值;a是CO2扩散过程中的同位素分馏,取4.4‰,b为CO2羧化过程中的同位素分馏,取27.4‰,此外,系数1.6表示空气中水蒸气与CO2的扩散率之比。Ca为大气二氧化碳浓度,大气二氧化碳浓度由全球系统研究实验室(https://ngdc.noaa.gov/ftp.html)提供。
1.4 统计方法
本文采用一元线性回归模型分析1969—2018年庐山日本柳杉WUE的动态变化趋势[32-33]。并采用曼−肯德尔(M-K)突变分析方法,研究庐山日本柳杉WUE的突变年份[34]。
为预测庐山日本柳杉水分利用效率未来变化趋势,利用Hurst指数(H)进行计算,H是定量描述时间序列的自相似性以及长程依赖性的方法,常采用R/S分析法[35]。本研究中R表示50年日本柳杉WUE序列的极差,S为该时间段WUE的标准差,R/S为极差与标准差的比值,ln为对数函数,τ为偶数序列。当0.5 < H < 1,表明时间序列变化具有持续性的序列,未来的变量与过去的变量是一致的关系;H = 0.5,说明时间序列为相互独立,不存在相互影响的随机序列;0 < H < 0.5,表明时间序列变化具有反持续性的序列,未来的变量与过去的变量是完全相反的序列。其中R2越接近1,显著性越强。植物在生长过程中,气候因子对其生长通常表现出一定的“滞后效应”[36],树木生长不仅受当年生长季气候因子的影响,还会受到上一年生长季后期气候因子变化的影响。因此,本研究选取上一年7月至当年12月共18个月份的气象数据进行相关性分析和多元回归分析。
2. 结果与分析
2.1 庐山地区各气候因子动态变化
通过对庐山1968—2018年各月气候因子的统计分析得到如图2的结果。从图2可以看出,干旱指数SPEI、WI以及SPI月变化基本一致。大致从2月到6月表现出下降的趋势,呈干旱趋势发展,SPEI和SPI在7月到10月波动较平缓,WI波动较大;干旱指数SPEI、WI以及SPI在12月呈上升趋势(图2a)。月平均气温从1月到7月呈上升趋势,最高气温出现在7月,为22.5 ℃;从8月到12月呈下降趋势,最低气温出现在1月,为0.3 ℃(图2b)。庐山地区的月平均太阳辐射和月平均风速最高出现在7月,为590.37 MJ/m2和4.94 m/s,月平均太阳辐射最低在1月,为285.72 MJ/m2,月平均风速最低在12月,为 3.53 m/s(图2c)。月平均降水量从1月到6月呈上升趋势,降水量最高出现在6月,为299.54 mm,最低出现在12月,为58.33 mm(图2d)。
2.2 庐山日本柳杉年轮稳定碳同位素值以及大气二氧化碳同位素值变化规律
如图3a所示,本研究中树轮δ13C序列没有因幼龄效应而表现出明显的趋势变化。日本柳杉δ13C序列变动范围在−23.09‰ ~ −25.67‰,年平均−24.55‰。这与O’Leary等[37]的研究得出自然条件下生长的陆地C3植物碳稳定同位素变化范围在−22‰ ~ −34‰的结论是相符的。庐山日本柳杉的δ13C总体呈递减趋势,平均每10年下降0.34‰。线性回归方程的相关系数R2 = 0.59,δ13C下降趋势显著。但在2001年后有小幅度上升趋势,最大值达到−24.35‰,在2010年呈下降趋势发展,最小值为−25.67‰。庐山δ13Cp序列(1969—2018)变动范围在−7.29‰ ~ −8.93‰(图3b),在1969—2018年总体上是逐年递减的趋势,线性回归方程的相关系数R2 = 0.98,下降趋势显著,平均每10年下降0.32‰。
2.3 庐山日本柳杉水分利用效率的变化特征
如图4a所示,1969—2018年间,庐山日本柳杉的WUE变动范围在91.06 ~ 118.89 μmol/mol,年平均值102.37 μmol/mol,总体呈现上升趋势,平均每10年上升5.2 μmol/mol,2013年出现最大值,为118.89 μmol/mol,最小值出现在1985年,为91.06 μmol/mol。为明确庐山日本柳杉WUE的年际变化特征,本研究对WUE进行了M-K突变分析和Hurst指数分析。从图4b的M-K突变分析可知:WUE呈低−高的趋势走向。1969—1987年,UF呈下降趋势,表明在这一时期,庐山日本柳杉WUE呈下降趋势,1988—2018年,UF呈上升趋势,表明庐山日本柳杉WUE呈上升趋势。庐山日本柳杉WUE的UF、UB交点出现在2004年(图4b),但庐山日本柳杉的WUE交点并不在±1.96临界线值范围内,没有通过0.05的检验,因此该年份的WUE交点上升不具有突变性。在双对数坐标系可以拟合得到年际庐山日本柳杉WUE的时间序列ln(R/S)与ln(τ/2)线性关系图(图4c)。由图4c可知,R/S趋势预测点之间存在良好的线性关系,R2 = 0.91,接近1,模型可行度高,线性拟合效果好。线性拟合的斜率为0.816 8,即Hurst指数估计值为0.816 8,表明庐山日本柳杉的WUE时间序列具有持续性关系,在未来变化中与过去存在较强的相关性,因此未来庐山日本柳杉的WUE呈现上升趋势。
![]() 图 4 庐山日本柳杉水分利用效率的变化特征及趋势WUE. 水分利用效率; UB.逆序时间序列变化;UF.顺序时间序列变化;R.极差;S.标准差;τ.偶数序列;ln.对数函数。WUE, water use efficiency; UB, inverse-order time series variation; UF, sequential time series variation; R, range; S, standard error; τ, even sequences; ln, logarithmic function.Figure 4. Variation characteristics and trends of water use efficiency of Cryptomeria japonica
图 4 庐山日本柳杉水分利用效率的变化特征及趋势WUE. 水分利用效率; UB.逆序时间序列变化;UF.顺序时间序列变化;R.极差;S.标准差;τ.偶数序列;ln.对数函数。WUE, water use efficiency; UB, inverse-order time series variation; UF, sequential time series variation; R, range; S, standard error; τ, even sequences; ln, logarithmic function.Figure 4. Variation characteristics and trends of water use efficiency of Cryptomeria japonica2.4 庐山日本柳杉水分利用效率与气候变化的相关分析以及多元回归模型解释
从庐山日本柳杉WUE序列与月气候变化的相关性分析(图5)可知:庐山日本柳杉WUE与各月气温大多呈正相关关系,与上年的7月、9—11月和当年的2—6月、9—11月呈显著正相关系,其中与上年的9月和当年的3—5月以及9月温度达到极显著正相关系;庐山日本柳杉WUE与各月太阳辐射大多呈负相关,但相关性不显著;WUE与干旱指数上年7—12月份、当年1—12月份干旱指数SPEI、SPI以及WI均呈负相关,但相关性不显著;庐山日本柳杉WUE与上年7—12月、当年1—12月风速均呈极显著负相关关系;WUE与上年7—12月至当年1—12月降水均无显著关系。在庐山日本柳杉的生长过程中, T和Ws在很大程度上驱动了日本柳杉水分利用效率的变化。通过多元线性回归方法将相关气候因子数值进行标准化来描述庐山日本柳杉水分利用效率与月气候因子之间的关系,回归过程选用逐步回归。得到庐山日本柳杉水分利用效率的回归方程。
![]() 图 5 庐山日本柳杉WUE与月气候变化的相关性P 为上年月份,C 为当年月份。**表示在置信度(双侧)为0.01时相关性显著;*表示在置信度(双侧)为0.05时相关性显著。P represents the month in previous year, C represents the month in current year. ** indicates a significant correlation at a confidence level (bilateral) of 0.01, * indicates that the correlation is significant at a confidence level (bilateral) of 0.05.Figure 5. Correlations between WUE of Cryptomeria japonica and monthly climate change in Lushan Mountain
图 5 庐山日本柳杉WUE与月气候变化的相关性P 为上年月份,C 为当年月份。**表示在置信度(双侧)为0.01时相关性显著;*表示在置信度(双侧)为0.05时相关性显著。P represents the month in previous year, C represents the month in current year. ** indicates a significant correlation at a confidence level (bilateral) of 0.01, * indicates that the correlation is significant at a confidence level (bilateral) of 0.05.Figure 5. Correlations between WUE of Cryptomeria japonica and monthly climate change in Lushan MountainWUE=58.349−3.733Ws1+1.487T3+1.690T9+1.667T−9−3.377Ws12(P<0.05,R2=0.65) 式中:WUE表示庐山日本柳杉水分利用效率,庐山日本柳杉水分利用效率主要与Ws1(当年1月风速)、T3(当年3月均温)、T9 (当年9月均温)、T−9(上年9月均温)、Ws12(当年12月风速) 相关。
3. 讨 论
3.1 干旱对日本柳杉水分利用效率的影响
水分利用效率是用来衡量植物个体或生态系统水平上碳水耦合关系的重要指标,能够揭示植物个体或生态系统WUE的变化特征[38]。WUE的影响因子随地区和尺度的不同而变化[39]。在本次研究中,本文选3个干旱指数进行庐山日本柳杉水分利用效率对干旱的响应验证发现,无论是SPEI、SPI还是WI,对庐山日本柳杉长期WUE的影响较小或者没有影响,均呈负相关关系(P > 0.05)。Song等[40]对西南亚热带常绿原生林水分利用效率研究表明亚热带常绿森林在干旱年的WUE呈增加趋势。一般认为,不同的生态系统WUE对干旱的响应是不同的。Liu等[41]对中国陆地生态系统水分利用效率与干旱响应研究发现在中国南方,中度和极端干旱会导致WUE下降,严重干旱往往导致WUE略有上升,而在东北和内蒙古中部地区轻微干旱通常会导致WUE增加。杜晓铮等[7]在研究陆地生态系统水分利用效率对气候变化的响应研究综述表明,在不同的气候区域干旱对WUE的影响有所差异,不同生态系统WUE对干旱的响应不同。有研究表明,干旱对植物的水分利用效率存在一定的滞后影响[42]。在本研究中发现,干旱对庐山日本柳杉WUE没有产生滞后影响。在湿润区,干旱发生的同时由于太阳辐射的射入,可能会加快植物的生长速度,同时蒸腾作用也会损失一部分的水分,造成植物WUE呈现出下降的趋势。在本次研究我们也发现,降水与 WUE呈负相关关系(P > 0.05),但相关性不显著。这可能是由于庐山地处湿润区,降水丰富,导致植物叶片气孔导度增大、蒸腾速率增强,造成了庐山日本柳杉水分利用效率的降低。
3.2 气温对日本柳杉水分利用效率的影响
温度对于植物水分利用的影响较为复杂。我们发现,气温对庐山日本柳杉的水分利用效率存在一定的滞后影响,上年的9月气温与庐山日本柳杉WUE呈显著正相关关系,当年的9月气温与庐山日本柳杉WUE也呈显著正相关关系。可能是由于气温适中,植物酶活性增强,从而影响植物水分利用。周佳等[43]利用树木年轮研究河南民权与陕西白水刺槐(Robinia pseudoacacia)水分利用效率对气候的响应表明,两地刺槐WUE与平均温度存在显著正效应关系。一定范围内,温度升高,叶片的气孔导度增加,植物的净光合速率大于蒸腾速率,造成植物WUE升高。崔茜琳等[44]利用MODIS数据研究青藏高原植被水分利用效率,青藏高原植被的WUE 与气温呈显著正相关关系,WUE的敏感性随气温的升高而增加。仇宽彪等[45]对陕西省各植被类型WUE研究时发现,在温度低于11 ℃的地区WUE和温度呈现显著正相关(P < 0.01),而高于11 ℃的地区两者之间没有显著关系(P > 0.05)。在不同的气候区, WUE对温度的响应存在着较大的差异。
3.3 风速对日本柳杉水分利用效率的影响
风会影响植物周围的环境,如降低空气的相对湿度和温度,并通过植物叶片遮挡影响太阳辐射的射入[46],同时会加速蒸腾速率而相应地降低植物的温度[47]。在不同的生态系统中,水分利用效率对Ws的响应幅度可能不同,甚至可能有完全不同的方向。王云霓[48]在研究宁夏六盘山典型树种水分利用效率中发现华北落叶松(Larix principis-rupprechtii)个体的WUE与Ws是正相关关系(P > 0.05)。在本次研究中发现,庐山日本柳杉WUE与Ws显著负相关关系,特别是当年的1月份和12月份的风速(P < 0.01),对庐山日本柳杉WUE产生了重要的影响。风速越大,植物的蒸腾作用会越强,植物体周围的空气湿度会降低,促使了植物体内的水分更快散失到大气中,造成植物WUE下降。在不同的地区,风速对于植物的WUE影响是有所差异的。庐山自然保护区风速呈现下降的趋势,平均每10年下降0.37 m/s,是日本柳杉WUE年际变化重要的影响因素之一。
3.4 太阳辐射对日本柳杉水分利用效率的影响
太阳辐射是植物光合作用所必须的重要元素之一,对植物WUE的变化也会产生重要影响。如徐晓桃[49]研究黄河源区植被的水分利用效率时发现,黄河源区的植被WUE与Rs是正相关关系。王云霓[48]研究宁夏六盘山典型树种华北落叶松时也发现WUE与Rs呈正相关关系,并且通过了显著性检验(P < 0.01)。一般认为,光照越强,植物的水分利用越高。但庐山日本柳杉WUE在本研究中与Rs未产生显著影响,这与他们的结果不同。一方面可能是由于太阳辐射增加时,植物的光合速率增大,但同时植物的蒸腾也在增大,WUE的变化难以确定。作为碳水循环的综合衡量指标,无论是植物个体的WUE或者是整个生态系统WUE,WUE的变化都是由多个相互作用的物理和生物过程决定,各个气候因子对WUE的变化具有相互协同作用。在评价树木WUE变化对气候因子的响应时,各个气候因子之间综合协同对WUE产生的影响还需进一步探究。
4. 结 论
本研究表明,1969—2018年期间,庐山日本柳杉树轮δ13C值呈下降趋势,WUE变化呈显著升高趋势。温度和风速是影响庐山日本柳杉WUE变化的主要气候因子,WUE与温度具有显著正相关关系,与风速具有显著负相关关系,并且温度对庐山日本柳杉WUE具有一定的滞后影响。而降水、太阳辐射以及干旱指数(SPI、SPEI、WI)对庐山日本柳杉年际WUE的变化未产生显著影响。本研究结果可为在全球气候变化下对庐山日本柳杉生长产生的影响提供理论依据,并且有助于庐山日本柳杉碳汇能力的评估以及提升杉木林的经营管理水平,同时为该地区杉木林生态系统的维护提供理论指导。
-
-
[1] 蒋瑾, 王康富, 张维静. 沙地凝结水及在水分平衡中作用的研究[J]. 干旱区研究, 1993, 10(2):1−9. Jiang J, Wang K F, Zhang W J. Study on condensation water of sandy land and its role in water balance[J]. Arid Zone Research, 1993, 10(2): 1−9.
[2] Zangvil A. Six years of dew observations in the Negev Desert, Israel[J]. Journal of Arid Environments, 1996, 32(4): 361−371. doi: 10.1006/jare.1996.0030.
[3] Kalthoffa N, Fiebig-Wittmaack M, Meiβner C, et al. The energy balance, evapo-transpiration and nocturnal dew deposition of an arid valley in the Andes[J]. Journal of Arid Environments, 2006, 65(3): 420−443. doi: 10.1016/j.jaridenv.2005.08.013.
[4] Malek E, McCurdy G, Giles B. Dew contribution to the annual water balances in semi-arid desert valleys[J]. Journal of Arid Environments, 1999, 42(2): 71−80. doi: 10.1006/jare.1999.0506.
[5] 郭晓楠, 查天山, 贾昕, 等. 典型沙生灌木生态系统凝结水量估算[J]. 北京林业大学学报, 2016, 38(10):80−87. Guo X N, Zha T S, Jia X, et al. Estimation of dewfall amount in a typical desert shrub ecosystem[J]. Journal of Beijing Forestry University, 2016, 38(10): 80−87.
[6] Scanlon B R, Milly P C D. Water and heat fluxes in desert soils(2): numerical simulations[J]. Water Resources Research, 1994, 30(3): 721−734. doi: 10.1029/93WR03252
[7] 曾亦键, 万力, 王旭升, 等. 浅层包气带地温与含水量昼夜动态的实验研究[J]. 地学前缘, 2006, 13(1):52−57. doi: 10.3321/j.issn:1005-2321.2006.01.008. Zeng Y J, Wan L, Wang X S, et al. An experimental study of day and night trends of soil temperature and moisture in the shallow unsaturated zone[J]. Earth Science Frontiers, 2006, 13(1): 52−57. doi: 10.3321/j.issn:1005-2321.2006.01.008.
[8] Jacobs A F G, Heusinkveld B G, Berkowicz S M. Dew deposition in a desert system: a simple simulation model[J]. Journal of Arid Environments, 1999, 42(3): 211−222. doi: 10.1006/jare.1999.0523
[9] Baguskas S A, King J Y, Fischer D T, et al. Impact of fog drip versus fog immersion on the physiology of bishop pine saplings[J]. Functional Plant Biology, 2017, 44(3): 339−350. doi: 10.1071/FP16234.
[10] 龚雪伟. 荒漠木本植物光合器官吸收冠层凝结水机理探究[D]. 乌鲁木齐: 新疆大学, 2017. Gong X W. A probe into the mechanisms of canopy dew uptake by photosynthetic organs of desert trees: based on molecular, cellular and physiological perspectives[D]. Urumqi: Xinjiang University, 2017.
[11] Wang X H, Xiao H L, Cheng Y B, et al. Leaf epidermal water-absorbing scales and their absorption of unsaturated atmospheric water in Reaumuria soongorica, a desert plant from the northwest arid region of China[J]. Journal of Arid Environments, 2016, 128: 17−29. doi: 10.1016/j.jaridenv.2016.01.005.
[12] Wang X H, Xiao H L, Ren J, et al. An ultrasonic humidification fluorescent tracing method for detecting unsaturated atmospheric water absorption by the aerial parts of desert plants[J]. Journal of Arid Land, 2016, 8(2): 272−283. doi: 10.1007/s40333-015-0018-z.
[13] Yan X, Zhou M X, Dong X C, et al. Molecular mechanisms of foliar water uptake in a desert tree[J]. AoB Plants, 2015, 7: 129.
[14] 庄艳丽, 赵文智. 荒漠植物雾冰藜和沙米叶片对凝结水响应的模拟实验[J]. 中国沙漠, 2010, 30(5):1068−1074. Zhuang Y L, Zhao W Z. Experimental study of effects of artificial dew on Bassia dasyphylla and Agriophyllum squarrosum[J]. Journal of Desert Research, 2010, 30(5): 1068−1074.
[15] Stone E C. Dew as an ecological factor(II): the effect of artificial dew on the survival of Pinus ponderosa and associated species[J]. Ecology, 1957, 38(3): 414−422. doi: 10.2307/1929884.
[16] Martin C E, Willert D J. Leaf epidermal hydathodes and the ecophysiological consequences of foliar water uptake in species of Crassula from the Namib Desert in Southern Africa[J]. Plant Biology, 2000, 2(2): 229−242. doi: 10.1055/s-2000-9163.
[17] Hill A J, Dawson T E, Shelef O, et al. The role of dew in Negev desert plants[J]. Oecologia, 2015, 178(2): 317−327. doi: 10.1007/s00442-015-3287-5.
[18] Goldsmith G R, Matzke N J, Dawson T E. The incidence and implications of clouds for cloud forest plant water relations[J]. Ecology Letters, 2013, 16(3): 307−314. doi: 10.1111/ele.12039.
[19] Fu P L, Liu W J, Fan Z X, et al. Is fog an important water source for woody plants in an Asian tropical karst forest during the dry season?[J]. Ecohydrology, 2016, 9(6): 964−972. doi: 10.1002/eco.1694.
[20] 郑玉龙, 冯玉龙. 西双版纳地区附生与非附生植物叶片对雾水的吸收[J]. 应用生态学报, 2006, 17(6):977−981. doi: 10.3321/j.issn:1001-9332.2006.06.005. Zheng Y L, Feng Y L. Fog water absorption by the leaves of epiphytes and non-epiphytes in Xishuangbanna[J]. Chinese Journal of Applied Ecology, 2006, 17(6): 977−981. doi: 10.3321/j.issn:1001-9332.2006.06.005.
[21] 郑新军, 李嵩, 李彦. 准噶尔盆地荒漠植物的叶片水分吸收策略[J]. 植物生态学报, 2011, 35(9):893−905. doi: 10.3724/SP.J.1258.2011.00893 Zheng X J, Li S, Li Y. Leaf water uptake strategy of desert plants in the Junggar Basin, China[J]. Chinese Journal of Plant Ecology, 2011, 35(9): 893−905. doi: 10.3724/SP.J.1258.2011.00893
[22] Vitarelli N C, Riina R, Cassino M F, et al. Trichome-like emergences in Croton of Brazilian highland rock outcrops: evidences for atmospheric water uptake[J]. Perspectives in Plant Ecology, Evolution and Systematics, 2016, 22: 23−35. doi: 10.1016/j.ppees.2016.07.002.
[23] Pina A L C B, Zandavalli R B, Oliveira R S, et al. Dew absorption by the leaf trichomes of Combretum leprosum in the Brazilian semiarid region[J]. Functional Plant Biology, 2016, 43(9): 851−861. doi: 10.1071/FP15337
[24] Eller C B, Lima A L, Oliveira R S. Foliar uptake of fog water and transport belowground alleviates drought effects in the cloud forest tree species, Drimys brasiliensis (Winteraceae)[J]. New Phytologist, 2013, 199(1): 151−162. doi: 10.1111/nph.12248.
[25] 岑宇, 刘美珍. 凝结水对干旱胁迫下羊草和冰草生理生态特征及叶片形态的影响[J]. 植物生态学报, 2017, 41(11):1199−1207. doi: 10.17521/cjpe.2017.0114. Cen Y, Liu M Z. Effects of dew on eco-physiological traits and leaf structures of Leymus chinensis and Agropyron cristatum grown under drought stress[J]. Chinese Journal of Plant Ecology, 2017, 41(11): 1199−1207. doi: 10.17521/cjpe.2017.0114.
[26] Zhuang Y L, Ratcliffe S. Relationship between dew presence and Bassia dasyphylla plant growth[J]. Journal of Arid Land, 2012, 4(1): 11−18. doi: 10.3724/SP.J.1227.2012.00011.
[27] Baguskas S A, Clemesha R E S, Loik M E. Coastal low cloudiness and fog enhance crop water use efficiency in a California agricultural system[J]. Agricultural and Forest Meteorology, 2018, 252: 109−120. doi: 10.1016/j.agrformet.2018.01.015.
[28] 林光辉. 稳定同位素生态学[M]. 北京: 高等教育出版社, 2013, 3−29. Lin G H. Stable Isotope Ecology [M]. Beijing: Higher Education Press, 2013, 3−29.
[29] West A G, Patrickson S J, Ehleringer J R. Water extraction times for plant and soil materials used in stable isotope analysis[J]. Rapid Communications in Mass Spectrometry, 2006, 20(8): 1317−1321. doi: 10.1002/rcm.2456.
[30] 刘文茹, 彭新华, 沈业杰, 等. 激光同位素分析仪测定液态水的氢氧同位素及其光谱污染修正[J]. 生态学杂志, 2013, 32(5):1181−1186. Liu W R, Peng X H, Shen Y J, et al. Measurements of hydrogen and oxygen isotopes in liquid water by isotope ratio infrared spectroscopy (IRIS) and their spectral contamination corrections[J]. Chinese Journal of Ecology, 2013, 32(5): 1181−1186.
[31] Schultz N M, Griffis T J, Lee X, et al. Identification and correction of spectral contamination in 2H/1H and 18O/16O measured in leaf, stem, and soil water[J]. Rapid Commun Mass Spectrom, 2011, 25(21): 3360−3368. doi: 10.1002/rcm.5236.
[32] Kim K, Lee X. Transition of stable isotope ratios of leaf water under simulated dew formation[J]. Plant, Cell & Environment, 2011, 34(10): 1790−1801.
[33] Guzmán-Delgado P, Earles J M, Zwieniecki M A. Insight into the physiological role of water absorption via the leaf surface from a rehydration kinetics perspective[J]. Plant, Cell & Environment, 2018, 41(8): 1886−1894.
[34] Emery N C. Foliar uptake of fog in coastal California shrub species[J]. Oecologia, 2016, 182(3): 731−742. doi: 10.1007/s00442-016-3712-4.
[35] Chamel A, Pineri M, Escoubes M. Quantitative determination of water sorption by plant cuticles[J]. Plant Cell and Environment, 1991, 14(1): 87−95. doi: 10.1111/j.1365-3040.1991.tb01374.x.
[36] Burgess S S O, Dawson T E. The contribution of fog to the water relations of Sequoia sempervirens (D. Don): foliar uptake and prevention of dehydration[J]. Plant, Cell and Environment, 2004, 27(8): 1023−1034. doi: 10.1111/j.1365-3040.2004.01207.x.
[37] 屠骊珠. 内蒙古西部地区九种旱生植物叶的解剖观察[J]. 内蒙古大学学报(自然科学版), 1982, 13(4):485−504. Tu L Z. Anatomical observations on nine xerophytes leaves in the west part of the Inner Mongolia[J]. Journal of Inner Mongolia University( Natural Science Edition), 1982, 13(4): 485−504.
[38] Yates D J, Hutley L B. Foliar uptake of water by wet leaves of Sloanea woollsii, an Australian subtropical rainforest tree[J]. Australian Journal of Botany, 1995, 43(2): 157−167. doi: 10.1071/BT9950157.
[39] Rundel P W. Water uptake by organs other than roots[J]. Physiological Plant Ecology II, 1982, 12: 111−134.
[40] Grammatikopoulus G, Manetas Y. Direct absorption of water by hairy leaves of Phlomis fruticosa and its contribution to drought avoidance[J]. Canadian Journal of Botany, 1994, 72(12): 1805−1811. doi: 10.1139/b94-222.
[41] Alvarado-Barrientos M S, Holwerda F, Asbjornsen H, et al. Suppression of transpiration due to cloud immersion in a seasonally dry Mexican weeping pine plantation[J]. Agricultural and Forest Meteorology, 2014, 186: 12−25. doi: 10.1016/j.agrformet.2013.11.002.
[42] Berry Z C, Smith W K. Cloud pattern and water relations in Picea rubens and Abies fraseri, southern Appalachian Mountains, USA[J]. Agricultural and Forest Meteorology, 2012, 162−163: 27−34. doi: 10.1016/j.agrformet.2012.04.005.
[43] 付晓玥. 阿拉善荒漠植物叶片性状研究[D]. 呼和浩特: 内蒙古大学, 2012. Fu X Y. Studies on leaf traits of Alashan desert plants[D]. Huhhot: Inner Mongolia University, 2012.
[44] 王春海. 中国藜属及近缘属植物的系统学研究[D]. 曲阜: 曲阜师范大学, 2015. Wang C H. Systematic study on Chenopodium and the related genera in China[D]. Qufu: Qufu Normal University, 2015.
[45] Goldsmith G R, Lehmann M M, Cernusak L A, et al. Inferring foliar water uptake using stable isotopes of water[J]. Oecologia, 2017, 184(4): 763−766. doi: 10.1007/s00442-017-3917-1.
[46] 范志超. 不同生境苦豆子种群生产性能与种子休眠特性研究[D]. 兰州: 兰州大学, 2016. Fan Z C. Study on productivity and seed dormancy characteristics of Sophora alopecuroides L. populations in different habitats[D]. Lanzhou: Lanzhou University, 2016.
-
期刊类型引用(3)
1. 陈彩云. 天然染料在鲜茧丝染色中的应用. 轻纺工业与技术. 2023(02): 145-147 .  百度学术
百度学术
2. 杨雨桐,张卿硕,符韵林,孙静. 巴里黄檀心材色素的提取及其抑菌活性. 东北林业大学学报. 2020(10): 100-103+119 .  百度学术
百度学术
3. 王敬贤. 木材染色技术研究进展. 林业科技. 2020(06): 42-47 .  百度学术
百度学术
其他类型引用(4)




 下载:
下载: