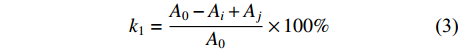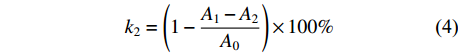Antioxidant activities in extracts from Pinus massoniana needles by deep eutectic solvents
-
摘要:目的 马尾松松针富含多酚、黄酮类化合物,具有多种活性功能。通过对马尾松松针的低共熔溶剂(DES)提取物的制备及其抗氧化活性进行研究,深度开发林下资源,获得与传统提取方式相比更加绿色环保、活性优良并且高效的制备方法。方法 采用超声波技术辅助低共熔溶剂提取马尾松松针中活性成分,首先通过对比提取效果对3种低共熔溶剂进行了筛选,进一步在选定的低共熔溶剂(氯化胆碱/葡萄糖)基础上,进行液料比、超声温度、超声时间、超声功率对提取效果影响的单因素试验。在单因素试验基础上,以多酚、黄酮得率为指标,响应面法优化主要工艺参数,对比提取物与传统醇提物对DPPH·、ABTS+·的清除能力以及还原能力的差异。结果 马尾松松针提取物的最佳提取工艺为:液料比为10 mL/g,超声温度为48 ℃,超声时间为60 min,超声功率为300 W。在此条件下,多酚得率为7.387%,黄酮得率为10.377%,回归模型拟合良好,与醇提物相比,低共熔溶剂提取物的抗氧化活性整体优于醇提物。结论 采用超声波技术辅助低共熔溶剂提取的马尾松松针提取物的得率显著高于普通醇提法,通过显著性分析比较得出DES提取物抗氧化活性显著优于醇提物。该方法绿色环保,可实现高效提取马尾松松针成分,并充分保持其生物活性,在提升马尾松的资源利用方面具有一定的意义。Abstract:Objective The pine needles of Pinus massoniana are rich in polyphenols and flavonoids with multiple active functions. In this paper, the preparation and antioxidant activity of the deep eutectic solvents (DES) extract of pine needles of P. massoniana were studied to deepen the exploitation of the undergrowth resources under tree crowns and to provide a more environmentally-friendly extraction method of active ingredients with more activities and higher efficiencies compared with traditional ways.Method Active ingredients were extracted from P. massoniana needles by ultrasonic technology under the assistance of DES. Firstly, three kinds of DES were screened by comparing the extraction effect. Then, based on the selected DES-choline chloride/glucose, a single factor test was conducted on the effect of liquid-solid ratio, ultrasonic temperature, ultrasonic time and ultrasonic power on the extraction effect. Based on single factor experiments, different capacities between DES extract and conventional ethanol extract to scavenge and reduce DPPH·, ABTS+· was compared with the yield of polyphenols and flavonoids taken as indexes and response surface method as the optimization of main process parameter.Result The optimal process to produce P. massoniana needle extract was: ratio of liquid to solid 10 mL/g, ultrasonic temperature 48 ℃, ultrasonic time 60 min, ultrasonic power 300 W, yield of polyphenol in the above condition 7.387%, yield of flavonoids in the above condition 10.377%, regression model fits well. The antioxidant activity of DES extract was overall better than that of the conventional ethanol extract.Conclusion Ultrasonic technology under the assistance of DES has higher yield of the P. massoniana needles extract compared with conventional extraction methods, and it has significant effect on the antioxidant activity compared with ethanol extraction method. So this method can provide efficient extraction of P. massoniana needles ingredients while fully maintaining the biological activity. So this method can provide efficient extraction of P. massoniana needles ingredients while fully maintaining the biological activity. It will be significant in the resource utilization of the P. massoniana.
-
Keywords:
- Pinus massoniana /
- deep eutectic solvent /
- flavonoid /
- polyphenol /
- antioxidant
-
马尾松(Pinus massoniana)为松属乔木,在我国分布甚广,从华东、华南到华中、西南均有分布,是一种重要的荒山造林树种。马尾松松针是主要药用部位,与其他松科植物相比,富含黄酮及多酚类化合物,此外还含有多糖、挥发油、木脂素、莽草酸等成分,具有抗氧化、抑菌防腐、降糖降血脂、抗癌和护肝的功效,多用于食品工业和医药领域[1-2]。
目前,松科植物活性成分的提取方法为有机溶剂浸提、以微波、超声波等辅助提取,乙醇为常用溶剂。徐丽珊等[3]通过对水提法和醇提法进行比较,发现水提法对提取松针黄酮类化合物的影响优于醇提法。张霞[4]以超声波辅助乙醇提取油松松针中的类黄酮,最高提取率为3.66%。战英等[5]通过微波辅助乙醇提取红松(Pinus koraiensis)松针总黄酮提取率为3.37%。王冉等[6]利用超声波辅助乙醇提取红松松针总黄酮,得率约为5.82%。赵玉红等[7]对樟子松(Pinus sylvestris)树皮中的松多酚进行提取,对比了有机溶剂提取法、超声波–复合酶法和超声辅助提取法对提取效果的影响,研究发现:目前的提取方法普遍存在溶剂消耗量大、提取效率低和提取物纯度低等问题,如水提后的粗提物中除含有目标产物黄酮类化合物外,还会混入一些可溶物,如氨基酸、多糖、蛋白质等,会大大影响产物的纯度。因此,探索一种选择性强、绿色高效的提取方法来实现松针中黄酮类和多酚类的快速提取十分必要。
Abbott等[8]于2003年在离子液体之后首次提出一种新型绿色溶剂—低共熔溶剂(deep eutectic solvent,DES),它保有离子液体的大部分优势,而且克服了其高毒性,高成本,生物降解性差等弊端。DES主要由氢键供体和氢键受体通过较强的分子间氢键作用相结合,使其具备特殊的理化性质,如可忽略的挥发性和黏度的可调整能力。此外,在提取天然产物的过程中,DES可以与目标物形成较强作用力的分子间氢键,使其具有优于传统溶剂的选择性和萃取能力,并且可提高不稳定的生物活性成分的稳定性[9-10]。刘珊等[11]以金钱草(Lysimachia christinae)为原料,通过共晶溶剂与超声结合提取黄酮,最终得到的黄酮提取率为7.198 mg/g。因此,在本实验中,采用超声辅助低共熔溶剂法在单因素和响应面优化设计实验的基础上,进一步调整和优化了马尾松针叶中黄酮类和多酚类化合物的提取工艺,以确定最佳提取条件;测试了从马尾松松针中提取的黄酮和多酚的抗氧化作用;同时,比较了乙醇提取法与超声辅助低共熔溶剂法提取能力的差异,为松针中活性物质的提取提供了一定的理论依据和实践基础。
1. 材料与方法
1.1 材 料
所用马尾松松针采集于2019年8月,湖南省祁阳县大江林场。DPPH·、ABTS+·、芦丁、没食子酸为标准品,纯度大于98%,其余所用试剂均为分析纯。
1.2 研究方法
1.2.1 原料处理
将鲜马尾松松针通过清洗去杂,干净的原料经自然风干及低温干燥,破碎为80目粉末,冷藏备用。
1.2.2 没食子酸标准曲线绘制与多酚得率计算
取10.0 mg没食子酸标准品配制成1 g/L的母液,分别取0.25、0.50、0.75、1.00、1.25 mL上述配制好的母液置于5个25 mL容量瓶中,用蒸馏水定容,得到0.01、0.02、0.03、0.04、0.05 g/L溶液。取上述5种溶液各1.00 mL,以1.00 mL蒸馏水作空白对照,再分别加入5.00 mL的0.2 mol/L福林酚溶液,摇匀,静置5 min后,再分别加入4.00 mL的10%碳酸钠溶液,摇匀后置于45 ℃水浴15 min。使用紫外分光光度计(北京普析通用),在波长为765 nm下测定上述溶液的吸光值,以没食子酸质量浓度(g/L)为横坐标(X1),吸光值(A)为纵坐标(Y1),绘制标准曲线[12]。得到线性回归方程:Y1 = 115.76X1 + 0.001 8,
R21 = 0.999 2。对提取液使用蒸馏水稀释,并按照上述方法进行多酚含量的测定,将测得的吸光度值带入回归方程,得到多酚质量浓度,并按照式(1)计算提取液中多酚得率:
y1=c1v1D11000m1×100% (1) 式中:y1为多酚得率,%;c1为回归方程计算出的提取液中多酚质量浓度,g/L;v1为提取前溶液体积,mL;m1为提取前松针质量,g;D1为提取液稀释倍数。
1.2.3 芦丁标准曲线绘制与黄酮得率计算
取5.0 mg芦丁标准品配置成0.1 g/L的母液,分别取2.00、4.00、6.00、8.00、10.00 mL上述配置好的母液置于容量瓶中,加入相应量70%乙醇使各容量瓶溶液总体积为10 mL。以70%乙醇作空白对照。再分别加入5%亚硝酸钠溶液1.00 mL,摇匀后静置6 min,再加入10%硝酸铝溶液1.00 mL,摇匀后静置6 min后加入10%氢氧化钠溶液10.00 mL,摇匀后加入70%乙醇定容,摇匀静置15 min。在波长为510 nm下测吸光值,以芦丁质量浓度(g/L)为横坐标(X2),吸光值(A)为纵坐标(Y2),绘制标准曲线[13]。得到线性回归方程:Y2 = 12.654X2 – 0.000 9,
R22 = 0.999 7。对提取液使用乙醇稀释,并按照上述方法进行黄酮含量的测定,将测得的吸光度值带入回归方程,得到黄酮质量浓度,并按照式(2)计算提取液中黄酮得率:
y2=c2v2D21000m2×100% (2) 式中:y2为黄酮得率,%;c2为回归方程计算出的提取液中黄酮质量浓度,g/L;v2为提取前溶液体积,mL;m2为提取前松针质量,g;D2为提取液稀释倍数。
1.2.4 低共熔溶剂的制备和选择
3种低共熔溶剂配制方案如表1,在恒温水浴锅中,保持温度在60 ~ 62 ℃,磁力搅拌1 h,冷却至室温。分别使用3种低共熔溶剂与马尾松松针以液料比10 mL/g混合,在300 W、44 ℃的超声条件下56 min,对黄酮和多酚进行提取。
表 1 不同类型低共熔溶剂配制方案Table 1. Different types of deep eutectic solvents低共熔溶剂 Deep eutectic solvent 溶剂体系构成 Composition of solvent system 摩尔比 Mole ratio 氢受体 Hydrogen acceptor 氢供体 Hydrogen bond donors 水 Water DES-1 氯化胆碱 Choline chloride 丙三醇 Glycerol 水 Water 1∶1∶4 DES-2 氯化胆碱 Choline chloride 葡萄糖 Glucose 水 Water 1∶1∶4 DES-3 氯化胆碱 Choline chloride 尿素 Carbamide 水 Water 1∶1∶4 1.2.5 超声波辅助低共熔溶剂提取马尾松松针活性成分的工艺研究
准确称取0.900 0 g马尾松松针粉于指形管中,以马尾松松针中多酚、黄酮得率为评价指标进行单因素试验,分别考察低共熔溶剂类型(DES-1、DES-2、DES-3)、液料比(8、10、12、14、16、18 mL/g),超声功率(240、270、300、330、360、390 W)、超声时间(30、45、60、75、90、105、120 min)、超声温度(30、35、40、45、50、55 ℃)对提取物得率的影响。
根据单因素实验结果,采用Box-Behnken试验设计方法,利用Design-Expert 8.0.6 trial设计4因素3水平的响应面工艺优化试验,对超声波辅助低共熔溶剂提取马尾松松针提取物的工艺参数进行优化。
1.2.6 松针提取物的抗氧化活性研究
1.2.6.1 DPPH·自由基清除率测定
在96孔板的孔中依次加入不同质量浓度梯度的样液50 μL以及稀释好的DPPH·溶液200 μL,充分混匀于517 nm波长下测定吸光值Ai。用200 μL 95%乙醇代替DPPH·溶液,测定吸光度值Aj。用50 μL 95%乙醇代替不同质量浓度梯度的样液,使用全波长酶标仪(BioTek Instruments, Inc.)测定吸光度值A0[14]。根据式(3)计算活性物质对DPPH·清除率:
k1=A0−Ai+AjA0×100% (3) 式中:k1为DPPH·清除率;Ai为样品液的吸光度值;Aj为样品空白管的吸光度值;A0为空白对照管的吸光度值。
1.2.6.2 ABTS+·自由基清除率测定
将7.4 mmol/L ABTS+·溶液与2.6 mmol/L过硫酸钾溶液按体积比1∶1混合,室温避光静置12 ~ 14 h,用pH7.4的PBS溶液稀释至在734 nm处吸光度值为(0.70 ± 0.02),备用。在96孔板中依次加入30 μL不同质量浓度梯度的样液,270 μL ABTS+·溶液,静置6 min,在734 nm处测吸光度值,得到A1。用30 μL pH7.4的PBS溶液代替样液,测定吸光度值,得到A0。用270 μL pH7.4 PBS溶液代替ABTS+·溶液,测定吸光度值,得到A2[14]。根据式(4)计算活性物质对ABTS+·清除率k2:
k2=(1−A1−A2A0)×100% (4) 式中:k2为ABTS+·清除率,%;A0为空白对照吸光度值;A1为样液吸光度值;A2为样液空白管吸光度值。
1.2.6.3 总还原力的测定
在5 mL离心管中依次加入0.5 mL不同质量浓度的样液,0.5 mL 0.2 mol/L pH6.6磷酸盐缓冲液,0.5 mL 1%铁氰化钾溶液,摇匀,50 ℃水浴20 min后,迅速冷却,再依次加入0.5 mL 10%三氯乙酸溶液,摇匀,在4 000 r/min条件下离心10 min。在96孔板中依次加入150 μL上述离心后不同质量浓度的上清液,150 μL蒸馏水,30 μL0.1%氯化铁溶液,混匀,静置10 min,在700 nm处测吸光度值[15]。
2. 结果与分析
2.1 低共熔溶剂种类的选择
以液料比10 mL/g、超声功率300 W、超声温度44 ℃、超声波辅助提取56 min作为多酚、黄酮的提取条件,3种不同低共熔溶剂对多酚、黄酮的得率的影响如表2所示。
表 2 提取溶剂对多酚、黄酮得率的影响Table 2. Effects of extraction solvent on yield of polyphenol and flavone低共熔溶剂种类
Types of deep eutectic solvents多酚得率
Polyphenol yield/%黄酮得率
Flavone yield/%DES-1 7.66AB 10.11A DES-2 8.07A 10.05A DES-3 7.38B 9.15A 注:同列数值后不同大写字母表示差异显著(P < 0.05)。Note: values in the same column followed by different capital letters mean that the difference is significant at P < 0.05 level. 由表2可知DES-2对多酚的提取效果最佳,这是由于DESs与多酚类化合物之间的氢键作用力[16],当氯化胆碱为氢受体,氢供体分别为多糖、多元醇类、酰胺类等化合物时,多糖类对马尾松松针中的多酚结构更适合提取[17];DES-1对黄酮的提取效果最佳,而DES-2与DES-1提取黄酮的得率接近,且该溶剂体系重复性良好,利于实验的重复进行。综上,选择DES-2即氯化胆碱和葡萄糖制备的低共熔溶剂作为对马尾松松针提取物的最佳提取溶剂。
2.2 提取单因素试验结果及分析
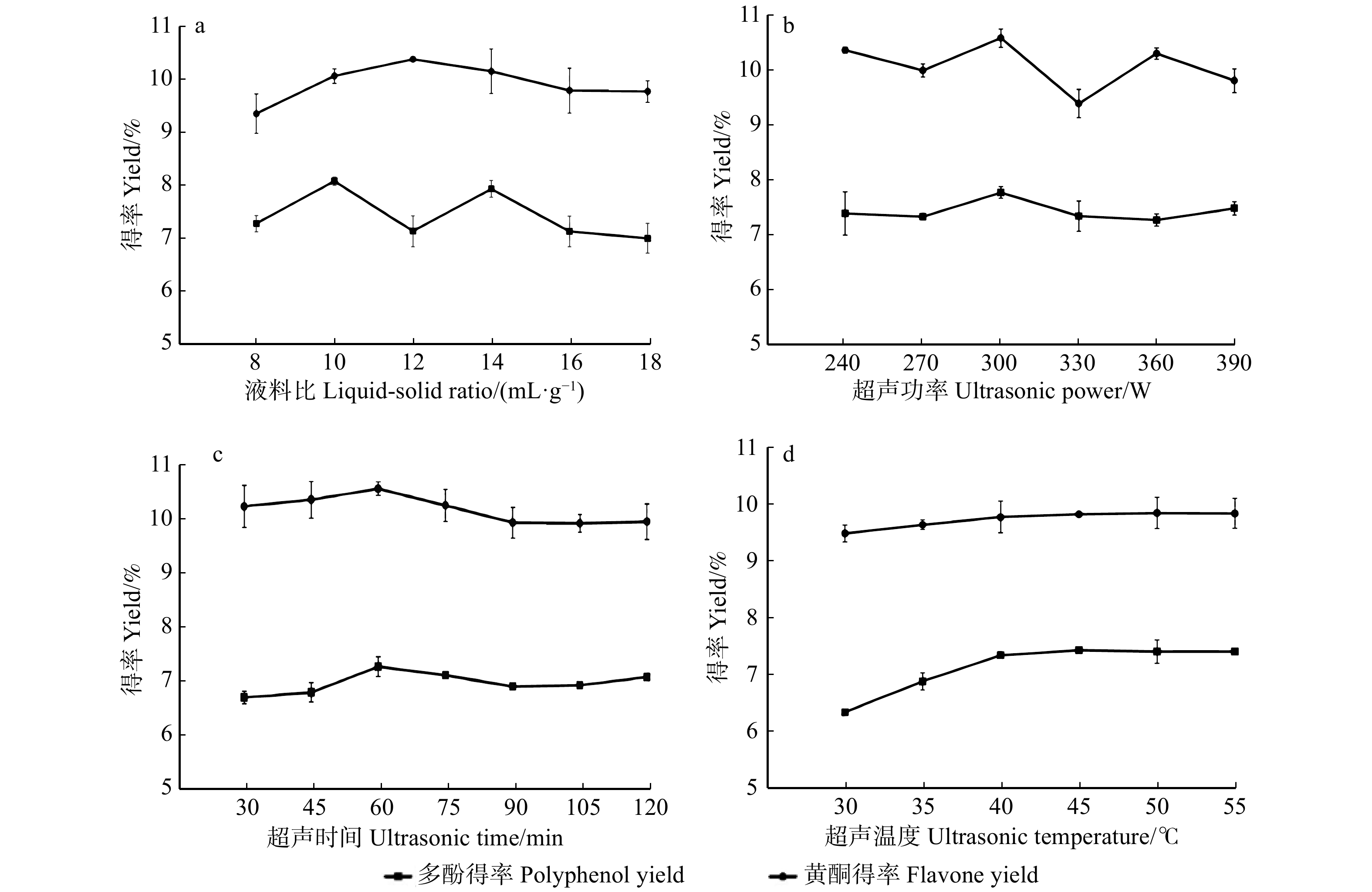
不同液料比、超声功率、超声时间、超声温度对马尾松松针提取物得率的影响,结果见图1。
由图1可知,随着液料比、超声功率、超声时间和超声温度的逐渐增加,松针提取物的得率总体趋势相似,先上升后下降,这可能是因为随着提取溶剂的增加,增大了原料与溶剂的接触面积,促使马尾松松针中的活性成分不断溶出并扩散至溶剂中,得率呈上升趋势;而前期实验增加超声功率和超声时间,则可以更充分地对马尾松松针组织的细胞壁进行破坏,与此同时温度的升高,也增加了马尾松松针中活性物质的溶出量。但当超声功率大于300 W,超声时间超过60 min和液料比大于10 mL/g时,继续改变因素水平值,提取物得率呈下降趋势或变化不显著,这可能是在超声时间较长或超声功率过高的情况下,组织的细胞壁不能够进一步被破坏,与此同时,已溶出的物质被破坏,导致得率降低。超声功率增加到330 W左右时,马尾松松针组织内的某些物质与黄酮类化合物一同被溶出,干扰黄酮含量测定,而后又被破坏,导致黄酮得率值未随功率的改变而呈现出规律性变化;当溶剂增加到一定程度时,萃取剂已将提取物充分提出,再继续增加溶剂可能导致提取物重新吸附到待提取物中,导致得率下降。
2.3 响应面实验结果及分析
2.3.1 响应面结果与方差分析
根据单因素的实验结果,分别以马尾松松针中多酚、黄酮得率为响应值,以液料比,超声功率,超声时间,超声温度为自变量,进行响应面分析实验,实验方案及结果如表3所示。
表 3 响应面实验方案及结果Table 3. Response surface design and experimental results试验号
Experiment No.液料比
Liquid-solid ratio/(mL·g−1)超声时间
Ultrasonic time/min超声温度
Ultrasonic temperature/℃超声功率
Ultrasonic power/W多酚得率
Polyphenol yield/%黄酮得率
Flavone yield/%1 10 60 35 270 6.367 9.132 2 8 60 55 300 6.186 9.919 3 12 60 35 300 6.459 9.773 4 10 75 45 330 6.465 9.126 5 8 75 45 300 6.628 9.071 6 10 60 55 330 6.828 9.593 7 10 60 35 330 6.569 9.303 8 8 60 45 330 6.361 8.892 9 10 45 45 270 6.465 9.889 10 8 60 45 270 6.485 8.691 11 12 60 55 300 6.922 10.184 12 10 60 45 300 7.571 10.548 13 10 45 35 300 6.027 9.830 14 10 60 55 270 6.511 10.120 15 10 60 45 300 7.617 10.245 16 10 45 55 300 6.655 9.633 17 10 60 45 300 7.513 10.364 18 8 60 35 300 6.204 8.633 19 10 75 35 300 6.454 8.316 20 8 45 45 300 5.969 9.771 21 10 75 55 300 6.897 9.303 22 12 60 45 330 6.127 9.694 23 10 75 45 270 6.741 9.600 24 12 75 45 300 6.279 9.979 25 10 60 45 300 7.686 10.390 26 10 45 45 330 6.384 9.936 27 12 60 45 270 6.721 9.109 28 10 60 45 300 7.277 10.054 29 12 45 45 300 5.636 10.192 多酚得率的变幅为5.636% ~ 7.686%,黄酮得率的变幅为8.316% ~ 10.548%,对实验数据进行回归拟合,得到马尾松松针多酚得率的回归方程y3、黄酮得率的回归方程y4和方差分析表(表4和表5)。
表 4 多酚方差分析表Table 4. Anova for response surface quadratic model of polyphenol方差来源 Variance source 平方和 Sum of squares 自由度 Degree of freedom 均方 Mean square F P 显著性 Significance 模型 Model 6.360 14 0.450 6.90 0.0004 ** A 8.060 × 10−3 1 8.060 × 10−3 0.12 0.7317 B 0.450 1 0.450 6.86 0.0202 * C 0.310 1 0.310 4.66 0.0487 * D 0.026 1 0.026 0.39 0.5418 AB 6.400 × 10−5 1 6.400 × 10−5 9.718 × 10−4 0.9756 AC 0.058 1 0.058 0.88 0.3646 AD 0.055 1 0.055 0.84 0.3753 BC 8.556 × 10−3 1 8.556 × 10−3 0.13 0.7239 BD 9.506 × 10−3 1 9.506 × 10−3 0.14 0.7097 CD 3.306 × 10−3 1 3.306 × 10−3 0.05 0.8259 A2 3.180 1 3.180 48.28 < 0.0001 ** B2 2.510 1 2.510 38.13 < 0.0001 ** C2 1.240 1 1.240 18.84 0.0007 ** D2 1.280 1 1.280 19.44 0.0006 ** 残差 Residual 0.920 14 0.066 失拟项 Lack of fit 0.820 10 0.082 3.37 0.1265 不显著 Not significant 纯误差 Pure error 0.098 4 0.024 总和 Total 7.290 28 注:**为差异极显著(P < 0.01),*为差异显著(P < 0.05)。下同。Notes:** means highly significant difference (P < 0.01), * means significant difference (P < 0.05). The same below. 表 5 黄酮方差分析表Table 5. Anova for response surface quadratic model of flavone方差来源 Variance source 平方和 Sum of squares 自由度 Degree of freedom 均方 Mean square F P 显著性 Significance 模型 Model 7.580 14 0.540 4.45 0.004 2 ** A 1.300 1 1.300 10.72 0.005 5 ** B 1.240 1 1.240 10.19 0.006 5 ** C 1.180 1 1.180 9.72 0.007 6 ** D 7.500 × 10−7 1 7.500 × 10−7 6.169 × 10−6 0.998 1 AB 0.059 1 0.059 0.49 0.496 4 AC 0.19 1 0.190 1.57 0.230 1 AD 0.037 1 0.037 0.30 0.590 5 BC 0.350 1 0.350 2.88 0.111 6 BD 0.068 1 0.068 0.56 0.467 3 CD 0.120 1 0.120 1.00 0.333 8 A2 1.080 1 1.080 8.91 0.009 8 ** B2 0.650 1 0.650 5.34 0.036 6 * C2 1.200 1 1.200 9.86 0.007 2 ** D2 1.700 1 1.700 13.96 0.002 2 ** 残差 Residual 1.700 14 0.120 失拟项 Lack of fit 1.570 10 0.160 4.64 0.076 3 不显著 Not significant 纯误差 Pure error 0.140 4 0.034 总和 Total 9.280 28 y3 = 7.53 + 0.026A + 0.19B + 0.16C – 0.046D – 4.000 × 10−3AB + 0.12AC – 0.12AD – 0.046BC – 0.049BD + 0.029CD – 0.70A2 – 0.62B2 – 0.44C2 – 0.44D2
式中:A为液料比(mL/g),B为超声时间(min),C为超声温度(℃),D为超声功率(W)。
y4 = 10.32 + 0.33A – 0.32B + 0.31C + 2.500 × 10−4D + 0.12AB – 0.22AC + 0.096AD + 0.30BC – 0.13BD – 0.17CD – 0.41A2 – 0.32B2 – 0.43C2 – 0.51D2
该回归模型的P = 0.000 4 < 0.01,有极显著差异,失拟项为0.126 5 > 0.05,差异不显著,模型稳定性较好,相关系数r = 0.873 5,Radj 2 = 0.746 9,说明拟合度良好;残差由随机误差引起,残差越小表明回归模型的拟合精度越高,由表4可知,该模型的残差为0.92,说明该模型有较好的拟合程度;纯误差越小表明实验过程中误差越低,该模型的纯误差为0.098,表明实验误差基本可忽略不计,可用于马尾松松针总多酚提取实验预测及结果分析。对回归模型显著性分析可知,因素A2、B2、C2、D2对多酚得率影响极显著(P < 0.01),因素B、C对多酚得率影响显著(0.01 < P < 0.05),因素A、D和交互项AB、AC、AD、BC、BD、CD因素相互交互作用对多酚得率的影响不显著(P > 0.05)。由表4模型的分析方差可得A、B、C、D 4个因素对多酚得率的影响顺序为B(超声时间) > C(超声温度) > D(超声功率) > A(液料比)。
该回归模型的P = 0.004 2 < 0.01,有极显著差异,失拟项为0.076 3 > 0.05,差异不显著,模型稳定性较好,相关系数r = 0.816 6,Radj 2 = 0.633 2,说明拟合度较好,残差为1.70,纯误差为0.14,表明该模型的拟合程度较高且实验误差可忽略不计,可用于马尾松松针总黄酮提取实验预测及结果分析。对回归模型显著性分析可知,因素A、B、C、A2、C2、D2对黄酮得率影响极显著(P < 0.01),B2对黄酮得率影响显著(0.01 < P < 0.05),交互项AB、AC、AD、BC、BD、CD因素的交互作用对黄酮得率的影响不显著(P > 0.05)。由表5模型的方差分析,可以得出A、B、C、D 4个因素对黄酮得率的影响顺序为:A(液料比) > B(超声时间) > C(超声温度) > D(超声功率)。
2.3.2 最佳条件确定和回归模型验证试验结果
通过响应面分析得到超声波辅助低共熔溶剂提取马尾松松针中多酚、黄酮最佳工艺条件为:液料比10.284 mL/g,超声时间59.87 min,超声温度47.65 ℃,超声功率298.63 W,在此条件下,多酚得率为7.539%,黄酮得率为10.406%,为实际操作中更便于控制,调整最佳工艺为:液料比10 mL/g,超声时间60 min,超声温度48 ℃,超声功率300 W。在此条件下进行最优工艺的验证,计算出多酚得率为7.387%,黄酮得率为10.377%,实际得率与模型预测值的误差分别为2.0%和0.2%,证明模型理论预测值与实际值拟合效果良好。
2.4 两种不同提取方法的松针提取物比较
2.4.1 醇提法制备马尾松松针提取物
精密称取1.0000 g马尾松松针粉,按照液料比50 mL/g加入60%乙醇,搅拌均匀,恒温水浴,50 ℃浸提60 min。抽滤,得到浸提液,再将浸提液旋转蒸发、冻干,得到醇提物冻干粉,冷藏,备用。
2.4.2 两种提取方法提取得率的评价
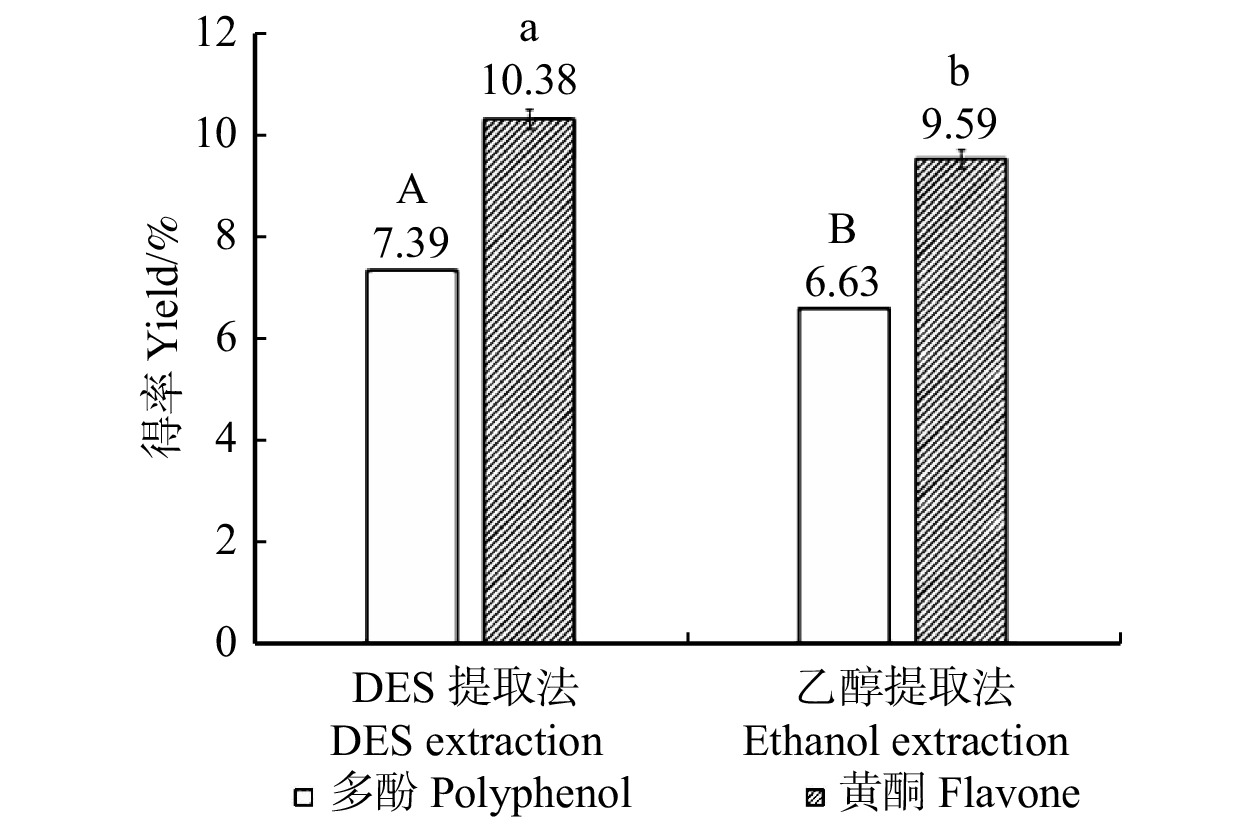
按照1.2.2和1.2.3的方法,对低共熔溶剂提取物和乙醇提取物进行多酚和黄酮得率的测定,结果如图2所示。由图2可知:在相同提取时间和提取温度条件下,低共熔溶剂和乙醇提取松针中多酚得率分别为7.39%、6.63%,黄酮得率分别为10.38%、9.59%。采用低共熔溶剂进行提取可得到更多的活性物质,溶剂用量少,价格低,可获得更高的得率,降低了制备成本,与乙醇溶剂提取相比,多酚和黄酮的得率分别提高了11%和8%。
2.4.3 两种松针提取物的抗氧化能力评价
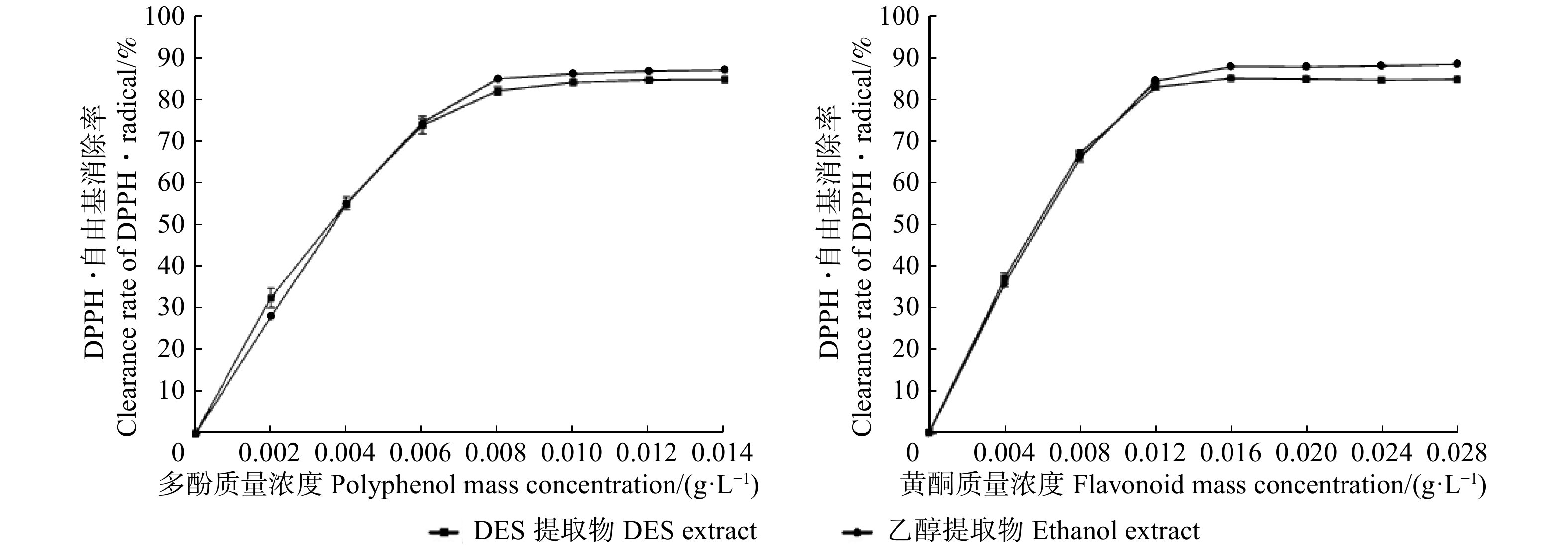
2.4.3.1 DPPH·自由基清除能力
低共熔溶剂提取物和醇提物对DPPH·清除能力对比曲线如图3所示。由图3可知:低共熔溶剂提取物和醇提物中活性成分对DPPH·的清除能力的剂量效应趋势差异不显著(P > 0.05)。低共熔溶剂提取物和乙醇提取物中多酚的IC50值分别为3.200、3.368 mg/L;黄酮的IC50值分别为4.950、5.197 mg/L,低共熔溶剂提取物对DPPH·自由基清除作用略高于乙醇提取物。
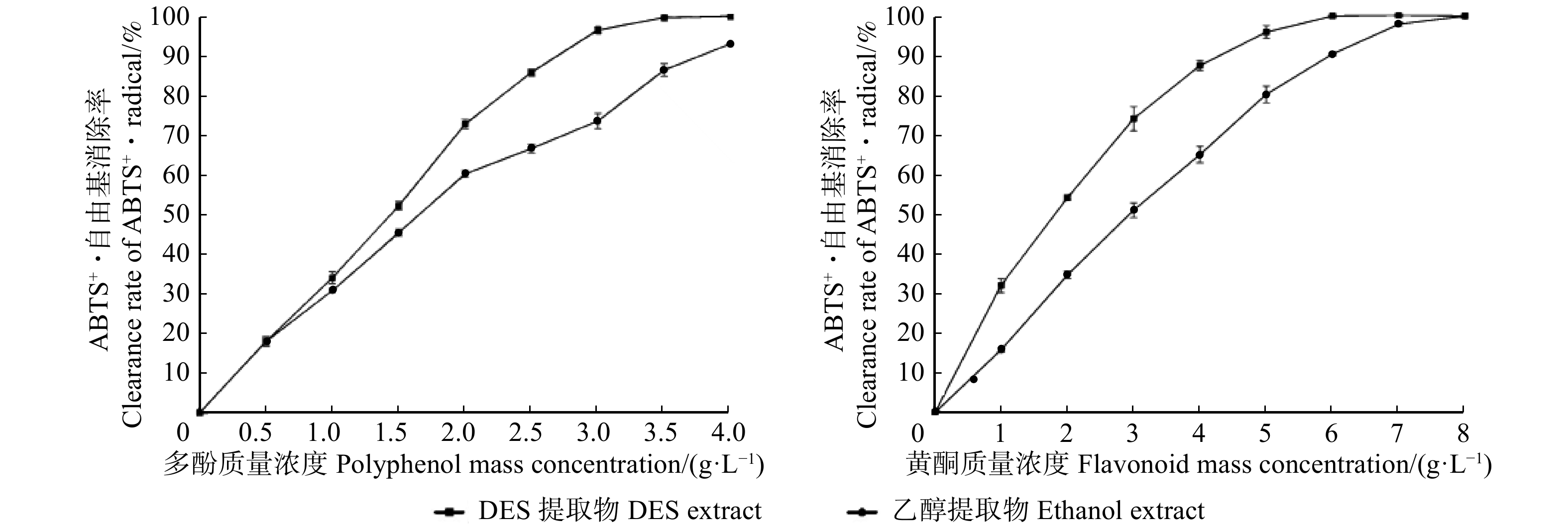
2.4.3.2 ABTS+·自由基清除能力
低共熔溶剂提取物和醇提物对ABTS+·清除能力对比曲线如图4。由图4可知:在试验质量浓度范围内,随着多酚、黄酮质量浓度的增加,清除率逐渐提升至平稳,且低共熔溶剂提取物中的活性成分清除能力更强,存在显著剂量–效应关系。通过计算,低共熔溶剂提取物和乙醇提取物中多酚的IC50值分别为1.217、1.506 mg/L;黄酮的IC50值分别为1.634、2.598 mg/L。综上,低共熔溶剂提取物对ABTS+·自由基清除效果显著优于乙醇提取物。
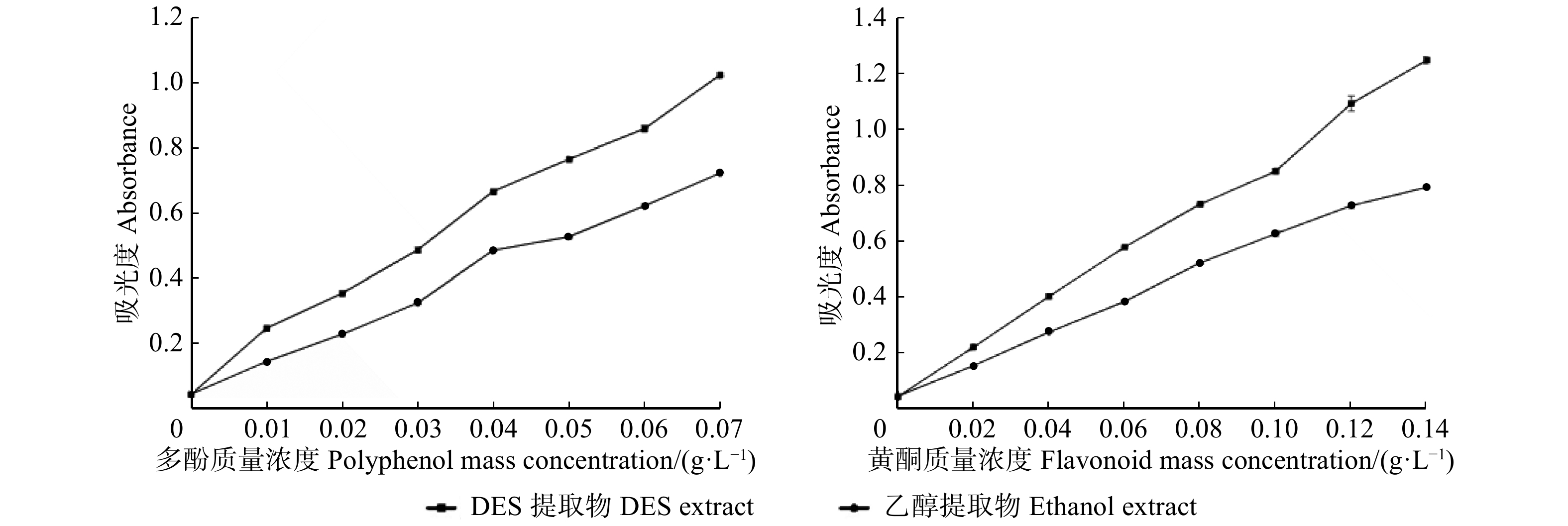
2.4.3.3 总还原力
低共熔溶剂提取物和醇提物总还原能力对比曲线如图5。还原力是评价物质抗氧化能力的重要指标,还原力越强,说明其清除自由基能力越强。由图5可知:在相同浓度梯度条件下,随着活性物质质量浓度提高,吸光度值所反映出来的还原能力越强,且低共熔溶剂提取物的还原能力均显著强于乙醇提取物(P < 0.05)。
3. 结 论
低共熔溶剂作为绿色环保的提取溶剂,具有提取效率高、构成简单、易采购、成本低、环保性和食品安全性良好的优势。本研究采用超声波辅助低共熔溶剂提取马尾松松针中多酚类化合物和黄酮类化合物,通过响应面优化出最佳工艺为:氯化胆碱–葡萄糖–水(摩尔比为1∶1∶4)、液料比10 mL/g、超声时间60 min、超声功率300 W、超声温度48 ℃。在此条件下,多酚得率为7.387%,黄酮得率为10.377%,较相同条件下的乙醇提取法,两种活性成分得率分别提高了11%和8%,溶剂使用量减少了5倍。
低共熔溶剂提取法能够良好保持提取物活性,通过与乙醇提取物对比DPPH·和ABTS+·的清除能力以及总还原能力,结果表明:低共熔溶剂提取物对自由基的清除能力和还原能力均强于醇提物,总还原能力和ABTS+·清除能力达到显著差异水平(P < 0.05)。这说明低共熔溶剂提取有效活性成分的能力更强,且对活性物质具有良好的保护性,不易破坏结构。
综上所述,低共熔溶剂作为一种可生物降解的新型绿色溶剂,由于黏度大、熔点高,在实践推广中还存在一定限制,本研究筛选的低共熔溶剂能实现较高的提取效率,黏度相对适宜,且提取物可采取树脂吸附方式实现纯化和脱溶,具备工业可实现性。马尾松松针中含有丰富的活性物质,且具有较强的抗氧化能力,在食品和药用方面具有很好的利用价值。采用新型提取方法制备的马尾松松针活性物质得率高,活性好,成本低,为马尾松资源的综合利用,开发高附加值产品,以及产业转化提供理论依据和研究基础。
-
表 1 不同类型低共熔溶剂配制方案
Table 1 Different types of deep eutectic solvents
低共熔溶剂 Deep eutectic solvent 溶剂体系构成 Composition of solvent system 摩尔比 Mole ratio 氢受体 Hydrogen acceptor 氢供体 Hydrogen bond donors 水 Water DES-1 氯化胆碱 Choline chloride 丙三醇 Glycerol 水 Water 1∶1∶4 DES-2 氯化胆碱 Choline chloride 葡萄糖 Glucose 水 Water 1∶1∶4 DES-3 氯化胆碱 Choline chloride 尿素 Carbamide 水 Water 1∶1∶4 表 2 提取溶剂对多酚、黄酮得率的影响
Table 2 Effects of extraction solvent on yield of polyphenol and flavone
低共熔溶剂种类
Types of deep eutectic solvents多酚得率
Polyphenol yield/%黄酮得率
Flavone yield/%DES-1 7.66AB 10.11A DES-2 8.07A 10.05A DES-3 7.38B 9.15A 注:同列数值后不同大写字母表示差异显著(P < 0.05)。Note: values in the same column followed by different capital letters mean that the difference is significant at P < 0.05 level. 表 3 响应面实验方案及结果
Table 3 Response surface design and experimental results
试验号
Experiment No.液料比
Liquid-solid ratio/(mL·g−1)超声时间
Ultrasonic time/min超声温度
Ultrasonic temperature/℃超声功率
Ultrasonic power/W多酚得率
Polyphenol yield/%黄酮得率
Flavone yield/%1 10 60 35 270 6.367 9.132 2 8 60 55 300 6.186 9.919 3 12 60 35 300 6.459 9.773 4 10 75 45 330 6.465 9.126 5 8 75 45 300 6.628 9.071 6 10 60 55 330 6.828 9.593 7 10 60 35 330 6.569 9.303 8 8 60 45 330 6.361 8.892 9 10 45 45 270 6.465 9.889 10 8 60 45 270 6.485 8.691 11 12 60 55 300 6.922 10.184 12 10 60 45 300 7.571 10.548 13 10 45 35 300 6.027 9.830 14 10 60 55 270 6.511 10.120 15 10 60 45 300 7.617 10.245 16 10 45 55 300 6.655 9.633 17 10 60 45 300 7.513 10.364 18 8 60 35 300 6.204 8.633 19 10 75 35 300 6.454 8.316 20 8 45 45 300 5.969 9.771 21 10 75 55 300 6.897 9.303 22 12 60 45 330 6.127 9.694 23 10 75 45 270 6.741 9.600 24 12 75 45 300 6.279 9.979 25 10 60 45 300 7.686 10.390 26 10 45 45 330 6.384 9.936 27 12 60 45 270 6.721 9.109 28 10 60 45 300 7.277 10.054 29 12 45 45 300 5.636 10.192 表 4 多酚方差分析表
Table 4 Anova for response surface quadratic model of polyphenol
方差来源 Variance source 平方和 Sum of squares 自由度 Degree of freedom 均方 Mean square F P 显著性 Significance 模型 Model 6.360 14 0.450 6.90 0.0004 ** A 8.060 × 10−3 1 8.060 × 10−3 0.12 0.7317 B 0.450 1 0.450 6.86 0.0202 * C 0.310 1 0.310 4.66 0.0487 * D 0.026 1 0.026 0.39 0.5418 AB 6.400 × 10−5 1 6.400 × 10−5 9.718 × 10−4 0.9756 AC 0.058 1 0.058 0.88 0.3646 AD 0.055 1 0.055 0.84 0.3753 BC 8.556 × 10−3 1 8.556 × 10−3 0.13 0.7239 BD 9.506 × 10−3 1 9.506 × 10−3 0.14 0.7097 CD 3.306 × 10−3 1 3.306 × 10−3 0.05 0.8259 A2 3.180 1 3.180 48.28 < 0.0001 ** B2 2.510 1 2.510 38.13 < 0.0001 ** C2 1.240 1 1.240 18.84 0.0007 ** D2 1.280 1 1.280 19.44 0.0006 ** 残差 Residual 0.920 14 0.066 失拟项 Lack of fit 0.820 10 0.082 3.37 0.1265 不显著 Not significant 纯误差 Pure error 0.098 4 0.024 总和 Total 7.290 28 注:**为差异极显著(P < 0.01),*为差异显著(P < 0.05)。下同。Notes:** means highly significant difference (P < 0.01), * means significant difference (P < 0.05). The same below. 表 5 黄酮方差分析表
Table 5 Anova for response surface quadratic model of flavone
方差来源 Variance source 平方和 Sum of squares 自由度 Degree of freedom 均方 Mean square F P 显著性 Significance 模型 Model 7.580 14 0.540 4.45 0.004 2 ** A 1.300 1 1.300 10.72 0.005 5 ** B 1.240 1 1.240 10.19 0.006 5 ** C 1.180 1 1.180 9.72 0.007 6 ** D 7.500 × 10−7 1 7.500 × 10−7 6.169 × 10−6 0.998 1 AB 0.059 1 0.059 0.49 0.496 4 AC 0.19 1 0.190 1.57 0.230 1 AD 0.037 1 0.037 0.30 0.590 5 BC 0.350 1 0.350 2.88 0.111 6 BD 0.068 1 0.068 0.56 0.467 3 CD 0.120 1 0.120 1.00 0.333 8 A2 1.080 1 1.080 8.91 0.009 8 ** B2 0.650 1 0.650 5.34 0.036 6 * C2 1.200 1 1.200 9.86 0.007 2 ** D2 1.700 1 1.700 13.96 0.002 2 ** 残差 Residual 1.700 14 0.120 失拟项 Lack of fit 1.570 10 0.160 4.64 0.076 3 不显著 Not significant 纯误差 Pure error 0.140 4 0.034 总和 Total 9.280 28 -
[1] 潘炘, 陈顺伟, 庄晓伟. 不同提取方式马尾松松针抗氧化能力研究[J]. 食品工业科技, 2009, 30(8):108−110. Pan X, Chen S W, Zhuang X W. Study on antioxidant activities in extracts from dry Pinus massoniana needles by different methods[J]. Science and Technology of Food Industry, 2009, 30(8): 108−110.
[2] 杨丽华. 马尾松松针抗氧化活性研究及其抗氧化功能饮料研制[D]. 广州: 广州医科大学, 2014. Yang L H. Research on antioxidant activity and antioxidant functional beverage of Masson pine needles[D]. Guangzhou: Guangzhou Medical University, 2014.
[3] 徐丽珊, 张萍华, 张瑜. 松针总黄酮的提取工艺优化研究[J]. 浙江师范大学学报(自然科学版), 2009, 32(2):207−211. Xu L S, Zhang P H, Zhang Y. Study on optimum process for extraction of flavonoids from pine needles[J]. Journal of Zhejiang Normal University (Natural Science), 2009, 32(2): 207−211.
[4] 张霞. 油松松针黄酮的分离提纯及其抗氧化活性研究[D]. 北京: 北京林业大学, 2010. Zhang X. Extraction and purification of flavonoids from pine needles and antioxidative activity of the extract[D]. Beijing: Beijing Forestry University, 2010.
[5] 战英, 陈丽娜, 石矛. 微波辅助提取红松松针总黄酮工艺优化[J]. 食品研究与开发, 2015, 36(16):69−72. doi: 10.3969/j.issn.1005-6521.2015.16.017 Zhan Y, Chen L N, Shi M. Optimization of process in extracting total flavonoids assisted by microwave from Korean pine needles[J]. Food Research and Development, 2015, 36(16): 69−72. doi: 10.3969/j.issn.1005-6521.2015.16.017
[6] 王冉, 李健, 黎晨晨, 等. 响应面法优化东北红松针总黄酮的超声辅助乙醇提取工艺[J]. 食品工业科技, 2018, 39(4):143−149. Wang R, Li J, Li C C, et al. Optimization of ultrasonic-assisted ethanol extraction of total flavonoids from Pinus koraiensis needles by response surface methodology[J]. Science and Technology of Food Industry, 2018, 39(4): 143−149.
[7] 赵玉红, 翟亚楠, 王振宇. 樟子松树皮中松多酚的提取工艺研究及提取方法比较[J]. 食品工业科技, 2013, 34(4):304−309. Zhao Y H, Zhai Y N, Wang Z Y. Extraction of polyphenols from Pinus sylvestris L. and comparison of extraction method[J]. Science and Technology of Food Industry, 2013, 34(4): 304−309.
[8] Abbott A P, Capper G, Davies D L, et al. Novel solvent properties of choline chloride/urea mixtures[J]. Chemical Communications, 2003, 9(1): 70−71.
[9] Dai Y T, Verpoorte R, Choi Y H. Natural deep eutectic solvents providing enhanced stability of natural colorants from safflower (Carthamus tinctorius)[J]. Food Chemistry, 2014, 159: 116−121. doi: 10.1016/j.foodchem.2014.02.155
[10] Dai Y T, Rozema E, Verpoorte R, et al. Application of natural deep eutectic solvents to the extraction of anthocyanins from Catharanthus roseus with high extractability andstability replacing conventional organic solvents[J]. Journal of Chromatography A, 2016, 1434: 50−56. doi: 10.1016/j.chroma.2016.01.037
[11] 刘珊, 李德慧, 孙科, 等. 新型绿色低共熔溶剂用于金钱草总黄酮的提取研究[J]. 时珍国医国药, 2019, 30(6):1312−1314. Liu S, Li D H, Sun K, et al. The research of new deep eutectic solvent extract total flavone from desmodium[J]. Lishizhen Medicine and Materia Medica Research, 2019, 30(6): 1312−1314.
[12] 胡文杰, 李阁, 李冠喜. 马尾松松针挥发油化学成分及抗氧化活性研究[J]. 中国粮油学报, 2018, 33(12):42−48. doi: 10.3969/j.issn.1003-0174.2018.12.008 Hu W J, Li G, Li G X. Study on chemical constituents and antioxidant activity of volatile oil from Pinus massoniana pine needles[J]. Journal of the Chinese Cereals and Oils Association, 2018, 33(12): 42−48. doi: 10.3969/j.issn.1003-0174.2018.12.008
[13] 彭映林, 谢丹, 李媛, 等. 黑茶中茶多酚的提取及其含量测定方法的研究进展[J]. 广东化工, 2019, 46(19):110−111, 138. Peng Y L, Xie D, Li Y, et al. Research progress on extraction and determination methods of tea polyphenols in dark tea[J]. Guangdong Chemical Industry, 2019, 46(19): 110−111, 138.
[14] 郭海欢. 刺玫果提取物化学成分分离及黄酮苷元的制备[D]. 吉林: 吉林化工学院, 2017. Guo H H. Study on component separation of the Rosa davurica Pall. extracts and flavonoid aglycones preparation[D]. Jilin: Jilin Institute of Chemical Technology, 2017.
[15] Farvin K H S, Andersen L L, Nielsen H H, et al. Antioxidant activity of cod (Gadus morhua) protein hydrolysates: in vitro assays and evaluation in 5% fish oil-in-water emulsion[J]. Food Chemistry, 2014, 149: 326−334. doi: 10.1016/j.foodchem.2013.03.075
[16] 倪玉娇, 赵春建, 李春英, 等. 超声辅助低共熔溶剂提取沙棘籽粕多酚的工艺优化[J]. 植物研究, 2017, 37(3):474−480. doi: 10.7525/j.issn.1673-5102.2017.03.020 Ni Y J, Zhao C J, Li C Y, et al. Process optimization of ultrasonic assisted deep eutectic solvents (DESs) extraction of polyphenols from Hippophae rhamnoides seed meal[J]. Plant Research, 2017, 37(3): 474−480. doi: 10.7525/j.issn.1673-5102.2017.03.020
[17] 谭婷. 低共熔溶剂的制备及其在一些食品和中药分析中的应用研究[D]. 南昌: 南昌大学, 2016. Tan T. Preparation of deep eutectic solvent and their applications in the analysis of some food and Chinese herbs[D]. Nanchang: Nanchang University, 2016.
-
期刊类型引用(13)
1. 黄瑜,张锡宇,赵海桃,石统帅,邱隽蒙,符群. 沙棘叶提取物的体外抗氧化及乙酰胆碱酯酶抑制能力. 精细化工. 2024(02): 391-400 .  百度学术
百度学术
2. 秦汝兰,吕重宁,王丹萍,关颖丽,张立秋. 不同初加工方法对大三叶升麻酚酸类化学成分及抗氧化活性影响. 人参研究. 2024(03): 36-41 .  百度学术
百度学术
3. 李海洋,袁峻,孙巍巍. 松针油再生沥青流变性能与再生机理研究. 林业工程学报. 2024(04): 147-153 .  百度学术
百度学术
4. 李子煜,吴婷,马帅楠,徐晓云. 不同干燥方式对西兰花茎和叶品质的影响. 食品科学. 2024(14): 179-188 .  百度学术
百度学术
5. 竹娟,王译晗,陈立莉,曲文鑫,刘荣. 芍药花提取物中黄酮的测定及其体外抗氧化和降脂活性研究. 天然产物研究与开发. 2024(11): 1838-1844+1899 .  百度学术
百度学术
6. 乔勤勤,安婉营,马静然,张乐乐,刘艳红. 预处理方式对荠菜干燥特性和品质的影响. 鞍山师范学院学报. 2024(06): 59-64 .  百度学术
百度学术
7. 石统帅,吴小杰,钟明旭,赵海桃,邱隽蒙,符群. 超声辅助双水相萃取黑果腺肋花楸果实抗氧化成分. 中南林业科技大学学报. 2023(01): 191-202 .  百度学术
百度学术
8. 张家旭,王信,董学凤,叶倩女,郭玉儿,彭腾腾,尹盼盼,李海燕,石晓峰. 电感耦合等离子体质谱(ICP-MS)法结合化学计量学分析比较6种松针中无机元素的含量. 中国无机分析化学. 2023(03): 278-285 .  百度学术
百度学术
9. 周佳悦,候艳丽,王凡予,郭庆启. 超声辅助低共熔溶剂提取红松树皮原花青素及动力学研究. 食品工业科技. 2023(14): 229-236 .  百度学术
百度学术
10. 张锡宇,黄瑜,石统帅,赵海桃,邱隽蒙,符群. 超声波-半仿生法提取桑叶黄酮及其活性的研究. 北京林业大学学报. 2023(09): 147-156 .  本站查看
本站查看
11. 问娟娟,刘浪浪,张少荟,高艳蓉,张爽. 基于低共熔溶剂提取黄酮类化合物研究进展. 精细化工中间体. 2023(05): 6-11 .  百度学术
百度学术
12. 周新宇,吕重宁,秦汝兰. 刺玫果中花色苷提取工艺优化及抗氧化性分析. 食品工业科技. 2022(04): 178-186 .  百度学术
百度学术
13. 罗文峰,陈金峰,陈坤进. 松针洗手液的研究. 广州化工. 2022(17): 60-62 .  百度学术
百度学术
其他类型引用(7)



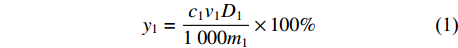
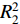
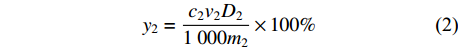
 下载:
下载: