Effects of pesticides on soil microbial population and preliminary screening of resistant strains
-
摘要:目的 筛选对乐果(有机磷类)、高效氯氰菊酯(菊酯类)和吡虫啉(新烟碱类)有抗药性的优势菌株,探究上述农药对土壤微生物种群生长的影响。方法 通过人为施药筛掉敏感菌,采用稀释涂布法和连续划线法分离纯化对农药有一定抗性的优势细菌进行表型特征和16SrDNA的鉴定。结果 从农药处理后的土壤中筛选到的优势细菌主要为芽孢杆菌属、金黄杆菌属、假单胞菌属和不动杆菌属4类:芽孢杆菌属中的C3菌株在高质量浓度4.000 g/L乐果和0.100 g/L的吡虫啉处理的土壤中不存在其菌落;不动杆菌属中的C5菌株在0.120 g/L和0.040 g/L的高效氯氰菊酯以及0.100 g/L吡虫啉处理组中均未发现该菌生长;假单胞菌属中的C6菌株在4.000 g/L的乐果及0.050 g/L和0.100 g/L的吡虫啉处理的土壤中无此菌株生长。不同质量浓度农药对土壤菌落均有不同程度的抑制。土壤中细菌和真菌菌落的抑制率与质量浓度之间呈正相关,且随时间推移,抑制率呈递减趋势,第14天仅有0.100 g/L吡虫啉处理组中的土壤细菌和真菌菌落数未恢复至正常水平;真菌中乐果和吡虫啉处理组间,第14天低质量浓度的土壤真菌菌落数显著(P < 0.05)高于高质量浓度的土壤菌落数。结论 土壤中存在对乐果、高效氯氰菊酯和吡虫啉农药有一定抗药性的优势细菌,为后续定向培育优良菌株提供理论基础;各农药的种类不同对土壤真菌和细菌菌落数量的抑制程度也有差异,其抑制程度为:吡虫啉 > 乐果 > 高效氯氰菊酯,且吡虫啉对土壤细菌数量抑制程度最高,对土壤真菌影响较小。Abstract:Objective The dominant strains with degradation ability to dimethoate (organic phosphorus), beta-cypermethrin (pyrethroids) and imidacloprid (neonicotinoid) were screened and the effects of the above pesticides on the growth of soil microbial populations were explored.Method The sensitive bacteria were screened out by artificial application, and the phenotypic characteristics and 16S rDNA of the dominant bacteria with certain resistance to pesticides were identified by dilution coating method and continuous streaking method.Result The dominant bacteria screened from the soil after pesticide treatment were mainly Bacillus, Chryseobacterium, Pseudomonas and Acinetobacter; C3 strain in Bacillus did not have colonies in the soil treated with 4.000 g/L dimethoate and 0.100 g/L imidacloprid at high mass concentrations; strain C5 of Acinetobacter did not grow in 0.120 g/L, 0.040 g/L beta-cypermethrin and 0.100 g/L imidacloprid treatment groups; strain C6 of Pseudomonas did not grow in 4.000 g/L dimethoate and 0.050 g/L and 0.100 g/L imidacloprid-treated soils. Different concentrations of pesticides had different degrees of inhibition on soil colonies. The inhibition rate of bacterial and fungal colonies in soil was positively correlated with the concentration, and the inhibition rate showed a decreasing trend over time. On the 14th day, only 0.100 g/L imidacloprid treatment group did not recover to the normal level. In the treatment groups of dimethoate and imidacloprid in fungi, the number of fungal colonies in the low concentration soils on the 14th day was significantly higher than that in the high concentration soils (P < 0.05).Conclusion There are dominant bacteria with certain resistance to dimethoate, beta-cypermethrin and imidacloprid pesticides in soils, which provide theoretical basis for directional culture of excellent strains. The inhibitory effects of different pesticides on the number of soil fungi and bacterial colonies are also different, and the inhibitory effects are as follows: imidacloprid > dimethoate > beta-cypermethrin. Moreover, imidacloprid has the highest inhibitory effect on the number of soil bacteria, and has little effect on soil fungi.
-
20世纪中叶,许多农药在施用后对环境造成的严重后果逐渐引起人们的关注[1]。由于农药在土壤中的高持久性及其对人体的毒性,农药残留及土壤污染成为了一个首要问题[2]。土壤微生物是土壤生态系统中最活跃的部分,是生态系统中物质循环的主要分解者和还原者,其群落的组成或活性对土壤肥力的保持具有重要意义。农药在施用后,大部分掉落于土壤中,从而对土壤微生物产生影响。研究农药对土壤微生物的影响,是评价农药对生态环境安全性的一个重要指标[3-4]。在土壤中农药和微生物起着交互作用,即农药在土壤中的降解离不开土壤微生物的作用。而微生物降解农药残留的研究起源于20世纪40年代,随着人们对环境的重视程度越来越高,对有机污染物降解过程和降解机理的研究有所深入。自然界中的部分微生物可以降解农药残留,且成本低,环境友好,不会造成二次污染,但效率相对较慢。由于自然环境复杂多变,也会影响微生物降解农药的效率[2]。但是在自然界中,也有大量适应性强、代谢类型不同的微生物。它们可以使用各种合成有机物,作为碳源,氮源和能量。这将有利于它们的生长,并且还可以通过各种代谢方式将有机农药完全矿化或降解成小的无毒分子,然后最终达到净化环境的目的[5]。例如假单胞菌属(Pseudomonas)、芽孢杆菌属(Bacillus)和青霉属(Penicillium)等优势降解菌存在于土壤中[6],克雷伯氏菌属(Klebsiella)、不动杆菌属(Acinetobacter)和芽孢杆菌属(Bacillus)等5种细菌能有效降解硫丹[7]以及芽孢杆菌属中的苏云金杆菌、蜡样芽胞杆菌等降解菌对氯霉素、链霉素和久效磷等具有抗药性[8],可发现细菌适应性强,在农药降解研究中占据主要地位。Zhang等[9]从4种土壤中分离出19株以青霉素和新霉素为唯一碳源的细菌菌株(变形杆菌门占84%、拟杆菌门占16%),且有3株细菌可以利用这些抗生素中含有的营养物质和能量来支持生长,因此部分细菌是含有抗药性基因和降解基因,将抗生素作为碳源,营养物质和能量助其生长代谢。在微生物降解残留农药的研究前期,多集中在对有机氯、有机磷农药的降解,随着拟除虫菊酯类以及新烟碱类农药在农业及林业上的大量应用,对这两类农药降解研究也逐渐多了起来。到目前为止,国内外的科研工作者已分离获得了许多可降解菊酯类及新烟碱类农药的微生物,包括细菌、真菌、放线菌3大类。经整理,目前已被分离获取的部分常用农药降解微生物及其能够分解的部分农药如表1所示。部分微生物虽然可对农药在土壤中的残留进行分解,但是农药对土壤微生物种群生长依然会产生或多或少的影响,如百菌清可导致土壤微生物数量和生物多样性的改变,它刺激了异养细菌和放线菌的生长,抑制了真菌的生长[24],Chen等[25]通过测定球孢白僵菌PfBb与5种市售杀虫剂(苦参碱、高效氯氰菊酯、吡虫啉、氟虫脲和氰氟虫腙)3个浓度(推荐的浓度、推荐浓度的20%和10%)的相容性和协同作用发现,与其他杀虫剂相比,10%推荐浓度的高效氯氰菊酯对球孢白僵菌PfBb菌丝生长的抑制作用最低,都可证明农药与微生物间的关系复杂多变。
表 1 部分微生物及其降解的部分农药种类Table 1. Some microorganisms and some pesticide types degraded by them微生物
Microorganism降解菌株
Degraded strain农药名称
Name of pesticide细菌
Bacteria假单胞菌属 Pseudomonas 甲胺磷 Methamidophos、2,4-D、DDT、敌敌畏 DDVP、二嗪农 Diazinon、地乐酚 Dinoseb、二硝甲酚 DNC、狄氏剂 Dieldrin、乐果 Dimethoate、敌稗 Propanil、林丹 Lindane、阿特拉津 Atrazine、1605、西玛津 Simazine、毒死蜱 Chlorpyrifos[10]、草甘膦 Glyphosate[11]、吡虫啉 Imidacloprid[12]、高效氯氰菊酯 Beta-cypermethrin[13] 芽孢杆菌属
Bacillus敌敌畏 DDVP、甲胺磷 Methamidophos、乐果 Dimethoate、甲基1605 Parathion-methyl、杀螟松 Sumithion、狄氏剂 Dieldrin、茅草枯2,2-dichloropropionic acid、DDT、毒莠定 Picloram、灭草隆 Monuron、吡虫啉 Imidacloprid[14]、高效氯氰菊酯Beta-cypermethrin[15] 不动杆菌属 Acinetobacter 乐果Dimethoate、PCB、敌敌畏DDVP、甲胺磷Methamidophos、1605、高效氯氰菊酯Beta-cypermethrin[16]、吡虫啉Imidacloprid[17] 金黄杆菌属 Chryseobacterium 草甘膦Glyphosate[18]、有机氯农药OCPs[19]、氟虫双酰胺Flubendiamide[20]、克百威Carbofuran[21]、多菌灵Carbendazim[22] 节杆菌属 Arthrobacter 茅草枯2,2-dichloropropionic acid、2,4-D、二嗪农Diazinon、毒莠定Picloram、西玛津Simazine、草藻灭Endothall、二甲四氯2-Methyl-4-chlorophenoxyacetic acid 土壤杆菌属
AgrobacterDDT、氯苯胺灵Chloropropham、茅草枯2,2-dichloropropionic acid、毒莠定Picloram 无色杆菌属
AchromobacterDDT、2,4-D、氯苯胺灵Chloropropham、2,4,5-T、PCB 黄杆菌属
Flavobacterium茅草枯2,2-dichloropropionic acid、毒莠定Picloram、三氯乙酸Trichloroacetic acid、氯苯胺灵Chloropropham、甲胺磷Methamidophos、2,4-D、灭草隆Monuron、1605 放线菌
Actinomycetes小单胞菌属
Micromonospora七氯Heptachlor、三氯乙酸Trichloroacetic acid 诺卡氏菌属
NocardiaDDT、2,4-D、七氯Heptachlor、茅草枯2,2-dichloropropionic acid、三氯乙酸Trichloroacetic acid、五氯硝基苯Pentachloronitrobenzene 链霉菌属
Streptomyces2,4,5-T、2,4-D、西玛津Simazine、DDT、茅草枯2,2-dichloropropionic acid、五氯硝基苯Pentachloronitrobenzene、二嗪农Diazinon 真菌
Fungi青霉
Penicillium七氯Heptachlor、五氯硝基苯Pentachloronitrobenzene、茅草枯2,2-Dichloropropionic acid、西玛津Simazine、毒莠定Picloram、灭草隆Monuron、除草醚Nitrofen、阿特拉津Atrazine、扑草津Prometryne、狄氏剂Dieldrin、敌稗Propanil、敌百虫Dipterex 曲霉
Aspergillus七氯Heptachlor、五氯硝基苯Pentachloronitrobenzene、2,4-D、敌百虫Dipterex、除草醚Nitrofen、扑草津Prometryne、敌蜱Propanil、毒莠定Picloram、西玛津Simazine、灭草隆Monuron 根霉属
Rhizopus七氯Heptachlor、地可松Fenaminosulf、阿特拉津Atrazine 毛霉属
Mucor五氯硝基苯Pentachloronitrobenzene、DDT 镰刀菌属
Fusarium阿特拉津Atrazine、DDT、艾氏剂Aldrin metabolized to dieldrin、西玛津Simazine、敌百虫Dipterex、七氯Heptachlor、五氯硝基苯Pentachloronitrobenzene 注:未标注文献的农药均来自文献 [23]。Note: pesticides not annotated are all from reference [23]. 红松(Pinus koraiensis)作为针叶树种,是我国国家二级重点保护野生植物,广泛分布于东北地区。由于森林采伐,大面积的天然林转变成人工林,病虫害的发生极为普遍,而农药的施用对这种森林类型的环境保护和生物多样性稳定等方面具有重要影响。Luo等[26]在评估色季拉山不同森林类型(栎树(Quercus spp.)、桦树(Betula spp.)、冷杉(Abies fabri)和云杉(Picea asperata)为主的森林)中有机氯农药(OCPs)从空气到地面的流通量发现,相比其他的林型,冷杉林更容易将OCPs从空气中转移到土壤中。Kylin等[27] 发现五氯苯酚(PCP)和五氯苯甲醚(PCA)在欧洲大陆的树种中能产生持久性有机污染的主要为松树。因此农药的施用对针叶林土壤微生物种群的影响具有重要研究意义。本研究选择乐果、高效氯氰菊酯和吡虫啉3种农药,开展对红松人工林地表层土壤中部分抗药性菌株的初步筛选及鉴定,并探讨其对红松人工林土壤微生物种群生长的影响,为红松人工林土壤中部分抗药性菌株的进一步筛选及菌株对农药降解能力的研究提供菌种资源和理论依据,且对后续优良菌株的定向培育提供理论基础。
1. 材料与方法
1.1 供试农药
本研究选用40%乐果(有机磷类)乳油(天津市河西区强力除四害药品加工厂),5.0%高效氯氰菊酯(菊酯类)乳油(黑龙江省平山林业制药厂)和3.0%吡虫啉(新烟碱类)悬浮剂(德强生物股份有限公司)3类农药。
1.2 供试土壤
供试土壤为8月份采自黑龙江省七台河市勃利县,林龄为15年,未施用任何农药的红松人工纯林,采用“S”型取样法,除去地面的枯枝落叶及砾石等杂质,取0 ~ 10 cm的土层混匀,将新鲜的土壤样品装入无菌聚乙烯袋密封,放置在盛有冰袋的整理箱中低温运回实验室[28],放入4 ℃冰箱中保存。部分土壤放入−20 ℃冰箱中备用。
1.3 主要培养基和试剂
主要培养基:牛肉膏蛋白胨液体(固体)培养基,马丁氏液体(固体)培养基。
主要试剂:无水乙醇(分析纯),购自国药集团化学试剂有限公司;细菌基因组DNA提取试剂盒,购自天根生化科技(北京)有限公司。
1.4 施用农药质量浓度
根据购买的高效氯氰菊酯、乐果和吡虫啉的使用说明,并结合中国农药信息网上的建议用量,根据说明书的推荐质量浓度将农药的质量浓度分别确定为推荐质量浓度、两倍及以上推荐质量浓度和二分之一及以下推荐质量浓度3种,如表2所示。
表 2 施用农药质量浓度Table 2. Mass concentration of pesticides appliedg/L 农药种类
Pesticide type低于推荐质量浓度
Lower than recommended
mass concentration推荐质量浓度
Recommended mass
concentration高于推荐质量浓度
Higher than recommended
mass concentration乐果 Dimethoate 1.333 2.000 4.000 吡虫啉 Imidacloprid 0.017 0.050 0.100 高效氯氰菊酯 Beta-cypermethrin 0.024 0.040 0.120 1.5 土壤处理及平板制备
本试验通过在土壤中按推荐质量浓度、低于推荐质量浓度和高于推荐质量浓度的标准,人为施药来筛选出对农药有一定抗性的优势细菌进行计数并鉴定。试验中分别对土壤进行3种不同药剂的处理和无菌水的对照(CK)处理。将上述备用土壤装入20 cm × 20 cm的养虫盒中,每盒100 g,均匀铺平,四周围上背光板,利用30 mL喷壶在养虫盒中均匀喷洒10 mL无菌水在室温下适应性培养7 d,后分别喷洒20 mL的表2中各质量浓度的农药及无菌水(CK),用牛皮纸封口,室温下避光培养。每组处理重复3次。
土壤中菌株的分离与纯化的实验操作均参照钱存柔等[29]方法:取喷洒农药后的1、7、14 d的土壤样品10 g放入装有玻璃珠的250 mL锥形瓶中,加入90 mL无菌水,200 r/min 30 ℃震荡30 min。采用稀释涂布法和连续划线法分离纯化菌株,将不同浓度的土壤菌悬液0.2 mL加入到灭菌后的平皿中,细菌所需的接种稀释度为10−3、10−4、10−5,真菌所需的接种稀释度为10−2、10−3、10−4。每个稀释质量浓度设3个重复。将接菌并冷却后的平板采用倒置培养的方式,细菌放入37 ℃恒温培养箱培养48 h,真菌于28 ℃恒温倒置培养72 h。并将纯化后菌株制作斜面留存备用。
平板菌落计数:对接种平板进行菌落计数,分别观察细菌和真菌在固体培养基上48和72 h的菌落,每个菌落为1个单位,称为菌落形成单位(cfu)[30]。部分细菌和真菌可在同一培养基上存在,因此利用显微镜观察菌落形态及连续划线法纯化菌株并进行计数,根据平板上菌落的数目,结合公式计算出每克含菌样品中所含的活菌总数,再与空白对照相比,计算出农药对细菌的平均抑制率。细菌取稀释度为10−3计数,真菌取稀释度为10−2进行计数。每克不同处理土壤中细菌/真菌的菌落总数(cfu/g) = 同一稀释度的菌落平均数 × 50 × 稀释倍数。
1.6 土壤中优势菌株表型特征和分子生物学鉴定
本文采用经典的表型特征和分子分类法中的16SrDNA序列测序,根据东秀珠等[31]及Buchanan等[32]的方法进行菌株鉴定。将纯化后的单一菌落放入已高温灭菌的装有50 mL液体牛肉膏蛋白胨培养基的锥形瓶中,以220 r/min,30 ℃在可控温摇床上培养48 h。
(1) 表型特征鉴定。主要采用了菌落形态和个体形态观察两个方面,革兰氏染色反应的实验操作参照钱存柔等[29]方法;菌落形态观察参照东秀珠等[31]和Buchanan等[32]的方法;鉴定细菌扫描电镜下的超微形态观察方法参照谢家仪等[33]的制备方法。
(2) 分子生物学鉴定。本试验利用试剂盒法提取DNA,按细菌DNA提取试剂盒(天根)方法提取各个菌株的基因组DNA,提取的DNA置于−20 ℃冰箱中保存备用。采用27F/1492R作为细菌引物(27F:5′-AGAGTTTGATCCTGGCTCAG-3′;1492R:5′-GGYTACCTTGTTACGACTT-3′)对分离菌种的目的区域进行扩增,将扩增后的PCR产物送至北京睿博兴科生物技术有限公司进行测序,测序结果提交NCBI进行同源序列比对。
1.7 数据处理
采用Microsoft Excel 2010进行数据统计、SPSS 20.0软件的单因素方差分析(One-way ANOVA)。
2. 结果与分析
2.1 土壤中主要优势菌株的筛选
通过人为施药后采用稀释涂布法和连续划线法,对不同质量浓度的各种农药处理后第1天的土壤中分离筛选出能生长出菌落的部分细菌。根据各菌株基本特征(表3、图1)观察,对各处理组土壤的菌株存在情况进行统计(表4),将菌株在各处理组,尤其在低、高质量浓度处理组土壤内存在情况,作为对优势菌株是否具有一定抗性的初步筛选标准,为后续定向培育优良菌株提供基础。
表 3 部分细菌基本特征Table 3. Basic characteristics of some bacteria菌株
Strain表型特征 Phenotypic characteristics 16SrDNA测序
16SrDNA sequencing菌落颜色
Colony color菌落特征
Colony characteristics革兰氏染色
Gram stain菌株形状
Strain shape芽孢
EndosporeBlast比对
Blast aligningC1 白色 White 不透明 Non-transparent 阳性 Positive 长杆状 Long rod-shaped 有 Exist 芽孢杆菌属 Bacillus C2 深黄色 Deep yellow 不透明 Non-transparent 阴性 Negative 长杆状 Long rod-shaped 无 Without 金黄杆菌属 Chryseobacterium C3 白色 White 半透明 Semi-transparent 阳性 Positive 长杆状 Long rod-shaped 有 Exist 芽孢杆菌属 Bacillus C4 白色 White 半透明 Semi-transparent 阴性 Negative 短杆状 Short rod-shaped 无 Without 假单胞菌属 Pseudomonas C5 无色 Colourless 透明 Transparent 阴性 Negative 球杆状 Ball and rod-shaped 无 Without 不动杆菌属 Acinetobacter C6 白色 White 半透明 Semi-transparent 阴性 Negative 短杆状 Short rod-shaped 无 Without 假单胞菌属 Pseudomonas C7 无色 Colourless 透明 Transparent 阴性 Negative 球杆状 Ball and rod-shaped 无 Without 不动杆菌属 Acinetobacter C8 淡黄色 Faint yellow 不透明 Non-transparent 阳性 Positive 长杆状 Long rod-shaped 有 Exist 芽孢杆菌属 Bacillus 表 4 各处理组土壤内部分优势菌株的存在情况Table 4. Presence of some dominant strains in the soil of each treatment group菌株
StrainCK 乐果 Dimethoate/(g·L−1) 高效氯氰菊酯 Beta-cypermethrin/(g·L−1) 吡虫啉 Imidacloprid/(g·L−1) 4.000 2.000 1.333 0.120 0.040 0.024 0.100 0.050 0.017 C1 * * * * * * * * * * C2 * * * * * * * * * * C3 * * * * * * * * C4 * * * * * * * * * * C5 * * * * * * * C6 * * * * * * * C7 * * * * * * * * * * C8 * * * * * * * 注:*表示该菌株存在。Note: * indicates the presence of strain. C1菌株(图1A、a)在琼脂平板上产生根状菌落,菌落为白色;C2菌株(图1B、b)在琼脂平板上产生边缘不整齐的深黄色菌落,菌株形状为长杆状;C3菌株(图1C、c)无根状菌落产生,在琼脂平板上形成边缘不整齐的白色菌落;C4菌株(图1D、d)和C6菌株(图1F、f)在琼脂平板上产生边缘不规整的白色菌落,菌株形状都为短杆状;C5菌株(图1E、e)和C7菌株(图1G、g)通过超微形态观察,C5菌株端部略尖,C7菌株端部钝圆,但都为球杆状;C8菌株(图1H、h)在琼脂平板上形成边缘不规则的淡黄色菌落。利用BLAST比对对各菌株进行鉴定(表3)发现,C1、C3和C8菌株属于芽孢杆菌属(Bacillus);C2菌株为金黄杆菌属(Chryseobacterium);C4和C6菌株属于假单胞菌属(Pseudomonas);C5和C7菌株为两株不动杆菌属(Acinetobacter)。
各菌株在各农药处理的土壤中存在情况如表4所示:C1、C2、C4和C7菌株在各处理组土壤中均存在;C3在3个不同质量浓度高效氯氰菊酯处理的土壤中均能生长菌落,在高质量浓度4.000 g/L乐果和0.100 g/L的吡虫啉处理的土壤中不存在其菌落生长;C5在不同质量浓度的乐果处理组中均能生长,在0.120和0.040 g/L的高效氯氰菊酯以及0.100 g/L吡虫啉处理组中均未发现该菌生长;C6在不同质量浓度的高效氯氰菊酯处理的土壤中均有其菌落的生长,但4.000 g/L的乐果及0.050和0.100 g/L的吡虫啉处理的土壤中无此菌株生长。C8在不同质量浓度的高效氯氰菊酯处理组中均未生长,在不同质量浓度的乐果和吡虫啉处理组中均能生长。
2.2 不同质量浓度农药对土壤微生物种群生长的影响
根据平板上菌落的数目,计算出每克含菌样品中所含的菌落总数。通过细菌菌落数与空白对照相比,计算出农药对细菌的平均抑制率,而真菌菌落数在不同天数的各农药处理组间的差异是利用SPSS20.0软件的单因素方差进行分析。
2.2.1 不同质量浓度农药对土壤细菌生长的影响
各农药对土壤中细菌生长影响的试验结果见表5。从表5中可以看出不同质量浓度农药对土壤中的细菌有一定程度的抑制,但随时间变化,其抑制率逐渐减弱。在0.100 g/L的吡虫啉处理土壤中,其第1天的细菌抑制率超过85%,第14天抑制率依然高于25%,其抑菌作用较为突出;各农药质量浓度不同,对土壤中菌落的抑制作用总体上随着浓度降低呈现下降趋势,并表现出明显的时间差异;3种农药的第1天的平均抑制率均高于第7天和第14天,第14天的抑制率基本为0或低于10%。
表 5 不同质量浓度农药对土壤细菌生长的影响(抑制率)Table 5. Effects of different mass concentrations of pesticides on soil microbial growth (inhibition rate)% 天数
Day number乐果
Dimethoate/(g·L−1)高效氯氰菊酯
Beta-cypermethrin/(g·L−1)吡虫啉
Imidacloprid/(g·L−1)4.000 2.000 1.333 0.120 0.040 0.024 0.100 0.050 0.017 1 68.60 34.45 19.21 74.09 61.28 51.83 86.89 71.95 44.51 7 37.62 20.48 3.33 37.14 27.62 15.71 60.95 45.24 18.1 14 6.33 0.00 0.00 0.00 0.00 0.00 25.95 3.80 0.00 注:菌落数大于对照组,则抑制率为0。Notes: the colony number is greater than the control group, and the inhibition rate is 0. 2.2.2 不同质量浓度农药对土壤真菌生长的影响
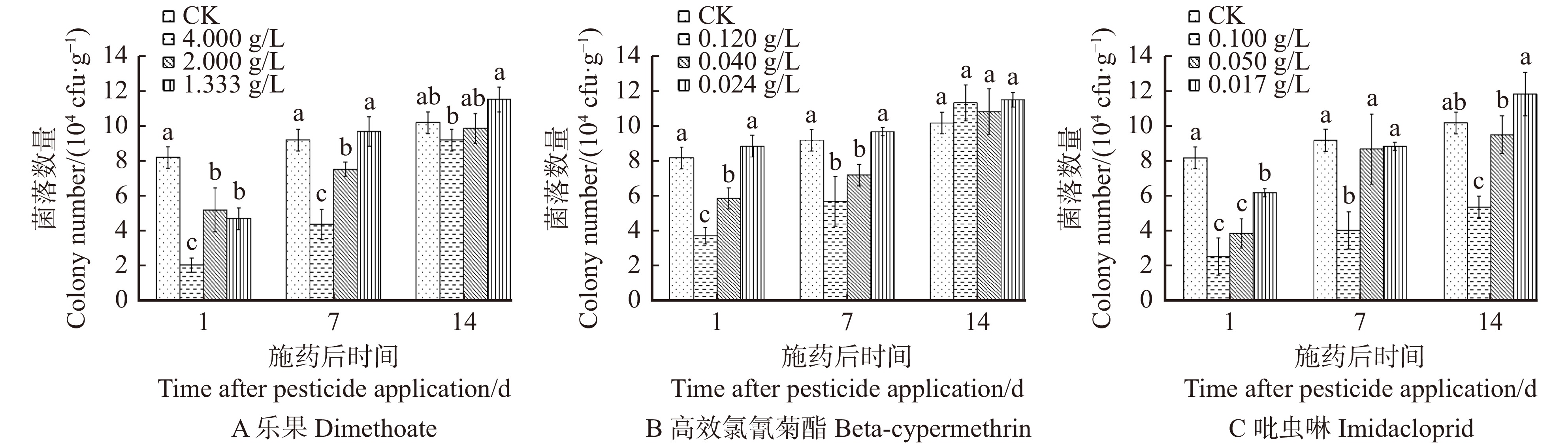
施用3种不同质量浓度(4.000、2.000和1.333 g/L)乐果处理组土壤的试验结果如图2A所示。其第1天的各处理组土壤真菌菌落数量与CK组之间均有显著差异(P < 0.05)。4.000 g/L乐果处理的土壤真菌菌落数量显著低于2.000和1.333 g/L乐果处理土壤中的真菌菌落数量(P < 0.05);2.000与1.333 g/L乐果处理组间的真菌菌落数量无显著差异(P > 0.05);第7天时乐果对土壤真菌菌落数量的抑制作用略有减弱,表现为4.000和2.000 g/L乐果处理的土壤真菌菌落数量均依然显著低于CK组(P < 0.05),但是1.333 g/L乐果处理组的真菌菌落数量恢复至正常水平,与CK组间无显著差异(P > 0.05);第14天时各处理组与CK组的土壤真菌菌落数量均无显著差异(P > 0.05)。但是,4.000 g/L乐果的真菌菌落数量略低于CK组,1.333 g/L乐果的真菌菌落数量略高于CK组,而且二者间有显著差异(P < 0.05)。
施用3种不同质量浓度(0.120、0.040和0.024 g/L)高效氯氰菊酯处理组土壤的试验结果如图2B所示。第1天的土壤真菌菌落数量中,0.120和0.040 g/L高效氯氰菊酯处理的土壤真菌菌落数量显著(P < 0.05)低于CK组,0.024 g/L高效氯氰菊酯处理组的真菌菌落数量与CK组间无显著差异(P > 0.05),各处理组间的土壤真菌菌落数量与质量浓度成反比,且具有显著差异(P < 0.05);第7天,0.120和0.040 g/L高效氯氰菊酯处理组,土壤真菌菌落数量依然显著(P < 0.05)低于CK组,0.024 g/L高效氯氰菊酯的真菌菌落数量与CK组间无显著差异(P > 0.05);第14天各处理组土壤真菌菌落数量均恢复正常,各处理组与CK组间无显著差异(P > 0.05)。
施用3种不同质量浓度(0.100、0.050和0.017 g/L)吡虫啉处理组土壤的试验结果如图2C所示。处理后第1天土壤的真菌菌落数量中,各处理组的土壤真菌菌落数量显著(P < 0.05)低于CK组,抑制效果显著。此时,0.017 g/L吡虫啉处理的土壤真菌菌落数量显著(P < 0.05)高于0.050和0.100 g/L吡虫啉处理组的土壤真菌菌落数量;第7天时,0.100 g/L吡虫啉处理的土壤真菌菌落数量呈被抑制状态,其土壤真菌菌落数量显著(P < 0.05)低于CK组的数量,0.050和0.017 g/L吡虫啉的真菌菌落数量已经恢复至正常水平;处理后第14天时,0.100 g/L吡虫啉的土壤真菌菌落数量依然呈显著受抑制状态,真菌菌落数量显著(P < 0.05)低于CK组,各处理组间的土壤真菌菌落数量与吡虫啉的质量浓度成反比,且差异显著(P < 0.05)。
3. 结论与讨论
土壤微生物与施入土壤中的农药之间存在着互作关系,一方面土壤中的微生物可以降解农药,另一方面农药又可以抑制或促进某些菌的生长。而土壤微生物是影响农药残留降解的首要因素,灭菌处理土壤中农药残留降解速率明显低于非灭菌土壤[34]。如今,生物降解法被认为是一种可有效去除农药的“绿色”解决方法[35]。由于细菌具有的多种适应能力和容易突变等特性,在农药降解微生物中占有主要地位。目前已经筛选获得菊酯类农药的降解菌主要有芽孢杆菌属、假单胞菌属等[36]。前人研究表明,假单胞菌属对有机磷类农药降解效果较好[37],芽孢杆菌属、节细菌属、链球菌属等对阿维菌素、菊酯类农药有高效降解的作用,链霉菌属对有机氯农药降解效果较好[38]。马青云等[39]研究发现一株金黄杆菌属具有优秀的烟嘧磺隆降解能力,在烟嘧磺隆污染环境的生物修复上具有较好的应用潜力。于晓菲等[40]筛选出一株能以高效氯氰菊酯为唯一碳源,7 d对100 mg/L的高效氯氰菊酯的降解率达到67.5%的芽孢杆菌属菌株,为降解高效氯氰菊酯及为农药残留的微生物修复奠定了基础。林启美等[41]研究了土壤根际解磷微生物数量和种群结构之间的关系,结果表明,解无机磷细菌主要为假单胞菌属菌株,解有机磷细菌主要有芽孢杆菌属和假单胞菌属的菌株,且解无机磷细菌比解有机磷细菌少。张爱民等[42]表示芽孢杆菌属和假单胞菌属对含磷的化合物都具有降解能力。刘亚冬[43]通过在土壤中施用新烟碱类杀虫剂发现芽孢杆菌属的相对丰富度比其CK增加了3.39%。因此,大量研究表明芽孢杆菌属、金黄杆菌属、假单胞菌属及不动杆菌属均可通过富集培养的方式成为某一领域或众多领域中的优势降解菌。何微等[44]从分离纯化出的54株细菌中筛选出了3株数量最多、长势良好短小芽孢杆菌、蜡样芽孢杆菌和巨大芽孢杆菌进行农残胁迫,发现在低质量浓度10 mg/L的农药中,其对农药的降解的效率较高,如对氧化乐果、对硫磷,其降解率可达100%,对其余农药的降解率在30% ~ 80%之间。在高质量浓度100 mg/L质量浓度的农药培养基中,菌株对氧化乐果、对硫磷的降解率下降至60% ~ 80%,对喹硫磷、啶虫脒、吡虫啉、毒死蜱降解率下降至28% ~ 51%。因此本试验通过观察优势细菌在不同浓度各农药处理土壤,尤其在低、高质量浓度处理土壤后第1天的菌落生长情况,进行初步的抗药性菌株筛选,发现金黄杆菌属的菌株的抗性最强,对不同浓度的各农药土壤处理后的环境具有较好的适应能力;芽孢杆菌属的菌株在不同质量浓度的各农药处理土壤中,均有菌株生长,特别是在不同质量浓度乐果和吡虫啉处理的土壤中3个菌株均能生长,说明芽孢杆菌属的抗药性较强,尤其对有机磷类和新烟碱类农药的抗性高于对菊酯类农药的抗性;而假单胞菌属的两株菌株在各农药的土壤处理中菌落生长情况并不相同,这可能是因为假单胞菌属对不同种类农药存在不同抗性,有的适宜在不同农药环境中生长,抗性较强;而另外菌株抗性较弱,对土壤环境有一定的选择性;不动杆菌属菌株的菌落生长的情况并不相同,其中C5不适宜在高效氯氰菊酯处理土壤中生长,而C7在各质量浓度的农药处理的土壤中,均发现该菌株的存在。而所筛选到的芽孢杆菌属、不动杆菌属、金黄杆菌属和假单胞菌属菌株在表1的可降解农药的细菌微生物中都存在,且根据前人研究发现部分细菌含有抗药性基因和降解基因[8-9],因此可以推断筛选的优势菌株可为后续定向培育优良菌株提供理论基础。
刘曼等[45]研究了氯氟氰菊酯浓度为0.3 mL/m2时水源涵养林土壤微生物数量的变化规律,在施药第7天,土壤微生物数量发生明显变化,细菌、放线菌数量明显降低,真菌数量增加。史婕等[46]通过3个水平上的土壤盆栽试验,研究了氯氰菊酯对紫色土土壤微生物数量。试验表明,氯氰菊酯对紫色土中的细菌的影响表现为“促进−抑制−恢复”,土壤真菌对氯氰菊酯极其敏感,处理后真菌数量显著降低,3周后恢复至对照水平。张清明等[47]应用室内模拟实验的方法研究发现低质量分数(0.4 μg/g)吡虫啉对土壤细菌数量有刺激作用,中质量分数(2.0 μg/g)和高质量分数(10.0 μg/g)吡虫啉对土壤细菌数量的影响表现为刺激—抑制作用,对土壤真菌影响较小。沙月霞[48]研究发现吡虫啉3 000倍稀释液在施用1 d后对土壤微生物群落功能多样性影响显著;在施用3 d后对土壤微生物群落功能多样性的影响仍然十分明显,施用后5 d影响力开始减弱;即使极低质量分数30 000倍稀释液的吡虫啉对枸杞土壤微生物群落多样性仍然会产生影响。因此,不同浓度的农药不光影响土壤微生物数量及多样性,还会影响降解菌株对农药的降解率。本试验利用不同质量浓度的各农药对土壤处理情况菌落均有不同程度的抑制。从表5和图2的柱状图可以看出,土壤中的细菌和真菌菌落数量在第1天受农药明显抑制,观察到第7天、第14天是可见,随时间推移,3种农药对细菌和真菌的抑制程度均呈递减趋势。同时发现,土壤内细菌菌落对吡虫啉极其敏感。该药剂处理后土壤中细菌数量显著降低,尤其在0.050 g/L的吡虫啉处理组中,可发现第7天时对细菌的抑制率依然达到45%以上。本试验各农药对土壤细菌和真菌菌落数量的抑制程度为:吡虫啉 > 乐果 > 高效氯氰菊酯,且吡虫啉对土壤细菌数量抑制程度最高,对土壤真菌影响较小。但在乐果和吡虫啉处理组中发现其土壤的真菌菌落数量,在第14天时低浓度的处理组中的土壤真菌菌落数显著高于高浓度的土壤菌落数,有可能是高浓度的乐果和吡虫啉筛掉土壤内的部分敏感真菌,导致其数量低于相对应的低浓度农药处理组的真菌数量。本研究结果可为后续优势菌株抗药性的进一步筛选及菌株对农药降解能力的研究提供理论依据。
-
表 1 部分微生物及其降解的部分农药种类
Table 1 Some microorganisms and some pesticide types degraded by them
微生物
Microorganism降解菌株
Degraded strain农药名称
Name of pesticide细菌
Bacteria假单胞菌属 Pseudomonas 甲胺磷 Methamidophos、2,4-D、DDT、敌敌畏 DDVP、二嗪农 Diazinon、地乐酚 Dinoseb、二硝甲酚 DNC、狄氏剂 Dieldrin、乐果 Dimethoate、敌稗 Propanil、林丹 Lindane、阿特拉津 Atrazine、1605、西玛津 Simazine、毒死蜱 Chlorpyrifos[10]、草甘膦 Glyphosate[11]、吡虫啉 Imidacloprid[12]、高效氯氰菊酯 Beta-cypermethrin[13] 芽孢杆菌属
Bacillus敌敌畏 DDVP、甲胺磷 Methamidophos、乐果 Dimethoate、甲基1605 Parathion-methyl、杀螟松 Sumithion、狄氏剂 Dieldrin、茅草枯2,2-dichloropropionic acid、DDT、毒莠定 Picloram、灭草隆 Monuron、吡虫啉 Imidacloprid[14]、高效氯氰菊酯Beta-cypermethrin[15] 不动杆菌属 Acinetobacter 乐果Dimethoate、PCB、敌敌畏DDVP、甲胺磷Methamidophos、1605、高效氯氰菊酯Beta-cypermethrin[16]、吡虫啉Imidacloprid[17] 金黄杆菌属 Chryseobacterium 草甘膦Glyphosate[18]、有机氯农药OCPs[19]、氟虫双酰胺Flubendiamide[20]、克百威Carbofuran[21]、多菌灵Carbendazim[22] 节杆菌属 Arthrobacter 茅草枯2,2-dichloropropionic acid、2,4-D、二嗪农Diazinon、毒莠定Picloram、西玛津Simazine、草藻灭Endothall、二甲四氯2-Methyl-4-chlorophenoxyacetic acid 土壤杆菌属
AgrobacterDDT、氯苯胺灵Chloropropham、茅草枯2,2-dichloropropionic acid、毒莠定Picloram 无色杆菌属
AchromobacterDDT、2,4-D、氯苯胺灵Chloropropham、2,4,5-T、PCB 黄杆菌属
Flavobacterium茅草枯2,2-dichloropropionic acid、毒莠定Picloram、三氯乙酸Trichloroacetic acid、氯苯胺灵Chloropropham、甲胺磷Methamidophos、2,4-D、灭草隆Monuron、1605 放线菌
Actinomycetes小单胞菌属
Micromonospora七氯Heptachlor、三氯乙酸Trichloroacetic acid 诺卡氏菌属
NocardiaDDT、2,4-D、七氯Heptachlor、茅草枯2,2-dichloropropionic acid、三氯乙酸Trichloroacetic acid、五氯硝基苯Pentachloronitrobenzene 链霉菌属
Streptomyces2,4,5-T、2,4-D、西玛津Simazine、DDT、茅草枯2,2-dichloropropionic acid、五氯硝基苯Pentachloronitrobenzene、二嗪农Diazinon 真菌
Fungi青霉
Penicillium七氯Heptachlor、五氯硝基苯Pentachloronitrobenzene、茅草枯2,2-Dichloropropionic acid、西玛津Simazine、毒莠定Picloram、灭草隆Monuron、除草醚Nitrofen、阿特拉津Atrazine、扑草津Prometryne、狄氏剂Dieldrin、敌稗Propanil、敌百虫Dipterex 曲霉
Aspergillus七氯Heptachlor、五氯硝基苯Pentachloronitrobenzene、2,4-D、敌百虫Dipterex、除草醚Nitrofen、扑草津Prometryne、敌蜱Propanil、毒莠定Picloram、西玛津Simazine、灭草隆Monuron 根霉属
Rhizopus七氯Heptachlor、地可松Fenaminosulf、阿特拉津Atrazine 毛霉属
Mucor五氯硝基苯Pentachloronitrobenzene、DDT 镰刀菌属
Fusarium阿特拉津Atrazine、DDT、艾氏剂Aldrin metabolized to dieldrin、西玛津Simazine、敌百虫Dipterex、七氯Heptachlor、五氯硝基苯Pentachloronitrobenzene 注:未标注文献的农药均来自文献 [23]。Note: pesticides not annotated are all from reference [23]. 表 2 施用农药质量浓度
Table 2 Mass concentration of pesticides applied
g/L 农药种类
Pesticide type低于推荐质量浓度
Lower than recommended
mass concentration推荐质量浓度
Recommended mass
concentration高于推荐质量浓度
Higher than recommended
mass concentration乐果 Dimethoate 1.333 2.000 4.000 吡虫啉 Imidacloprid 0.017 0.050 0.100 高效氯氰菊酯 Beta-cypermethrin 0.024 0.040 0.120 表 3 部分细菌基本特征
Table 3 Basic characteristics of some bacteria
菌株
Strain表型特征 Phenotypic characteristics 16SrDNA测序
16SrDNA sequencing菌落颜色
Colony color菌落特征
Colony characteristics革兰氏染色
Gram stain菌株形状
Strain shape芽孢
EndosporeBlast比对
Blast aligningC1 白色 White 不透明 Non-transparent 阳性 Positive 长杆状 Long rod-shaped 有 Exist 芽孢杆菌属 Bacillus C2 深黄色 Deep yellow 不透明 Non-transparent 阴性 Negative 长杆状 Long rod-shaped 无 Without 金黄杆菌属 Chryseobacterium C3 白色 White 半透明 Semi-transparent 阳性 Positive 长杆状 Long rod-shaped 有 Exist 芽孢杆菌属 Bacillus C4 白色 White 半透明 Semi-transparent 阴性 Negative 短杆状 Short rod-shaped 无 Without 假单胞菌属 Pseudomonas C5 无色 Colourless 透明 Transparent 阴性 Negative 球杆状 Ball and rod-shaped 无 Without 不动杆菌属 Acinetobacter C6 白色 White 半透明 Semi-transparent 阴性 Negative 短杆状 Short rod-shaped 无 Without 假单胞菌属 Pseudomonas C7 无色 Colourless 透明 Transparent 阴性 Negative 球杆状 Ball and rod-shaped 无 Without 不动杆菌属 Acinetobacter C8 淡黄色 Faint yellow 不透明 Non-transparent 阳性 Positive 长杆状 Long rod-shaped 有 Exist 芽孢杆菌属 Bacillus 表 4 各处理组土壤内部分优势菌株的存在情况
Table 4 Presence of some dominant strains in the soil of each treatment group
菌株
StrainCK 乐果 Dimethoate/(g·L−1) 高效氯氰菊酯 Beta-cypermethrin/(g·L−1) 吡虫啉 Imidacloprid/(g·L−1) 4.000 2.000 1.333 0.120 0.040 0.024 0.100 0.050 0.017 C1 * * * * * * * * * * C2 * * * * * * * * * * C3 * * * * * * * * C4 * * * * * * * * * * C5 * * * * * * * C6 * * * * * * * C7 * * * * * * * * * * C8 * * * * * * * 注:*表示该菌株存在。Note: * indicates the presence of strain. 表 5 不同质量浓度农药对土壤细菌生长的影响(抑制率)
Table 5 Effects of different mass concentrations of pesticides on soil microbial growth (inhibition rate)
% 天数
Day number乐果
Dimethoate/(g·L−1)高效氯氰菊酯
Beta-cypermethrin/(g·L−1)吡虫啉
Imidacloprid/(g·L−1)4.000 2.000 1.333 0.120 0.040 0.024 0.100 0.050 0.017 1 68.60 34.45 19.21 74.09 61.28 51.83 86.89 71.95 44.51 7 37.62 20.48 3.33 37.14 27.62 15.71 60.95 45.24 18.1 14 6.33 0.00 0.00 0.00 0.00 0.00 25.95 3.80 0.00 注:菌落数大于对照组,则抑制率为0。Notes: the colony number is greater than the control group, and the inhibition rate is 0. -
[1] 赵亮. 阿维菌素和高效氯氰菊酯在黄瓜地中的残留行为及其在土壤中的吸附[D]. 长沙: 湖南农业大学, 2013. Zhao L. Residual behavior of avermectin and beta cypermethrin in cucumber field and its adsorption in five kinds of soil tested [D]. Changsha: Hunan Agricultural University, 2013.
[2] Bhandari G, Atreya K, Scheepers P T J, et al. Concentration and distribution of pesticide residues in soil: non-dietary human health risk assessment [J/OL]. Chemosphere, 2020, 253: 126594[2021−11−05]. https://doi.org/10.1016/j.chemosphere.2020.126594.
[3] 陈峻峰, 李刚, 谭秀益, 等. 不同浓度甲维盐·毒死蜱对土壤微生物量及呼吸强度的影响[J]. 湖南农业科学, 2013(5): 60−63. Chen J F, Li G, Tan X Y, et al. Effects of different concentrations of emamectin-benzoate and chlorpyrifos on microbial biomass and respiratory intensity in soil[J]. Hunan Agricultural Sciences, 2013(5): 60−63.
[4] 唐美珍, 郭正元. 68%代森锰锌对土壤微生物种群及呼吸作用的影响[J]. 土壤通报, 2010, 41(6): 1365−1369. Tang M Z, Guo Z Y. Effect of 68% mancozeb on soil microorganism’s population and respiratio[J]. Chinese Journal of Soil Science, 2010, 41(6): 1365−1369.
[5] Huang Y, Xiao L, Li F, et al. Microbial degradation of pesticide residues and an Emphasis on the degradation of cypermethrin and 3-phenoxy benzoic acid: a review[J/OL]. Molecules, 2018, 23(9): 2313[2021−12−11]. https://pubmed.ncbi.nlm.nih.gov/30208572/.
[6] Prudnikova S, Streltsova N, Volova T. The effect of the pesticide delivery method on the microbial community of field soil[J]. Environmental Science and Pollution Research, 2021, 28(7): 8681−8697. doi: 10.1007/s11356-020-11228-7
[7] Kafilzadeh F, Ebrahimnezhad M, Tahery Y. Isolation and identification of endosulfan-degrading Bacteria and evaluation of their bioremediation in Kor River, Iran[J]. Osong Public Health and Research Perspectives, 2015, 6(1): 39−46. doi: 10.1016/j.phrp.2014.12.003
[8] Rangasamy K, Athiappan M, Devarajan N, et al. Emergence of multi drug resistance among soil bacteria exposing to insecticides[J]. Microbial Pathogenesis, 2017, 105: 153−165. doi: 10.1016/j.micpath.2017.02.011
[9] Zhang Q, Dick W A. Growth of soil bacteria, on penicillin and neomycin, not previously exposed to these antibiotics[J]. Science of the Total Environment, 2014, 493: 445−453. doi: 10.1016/j.scitotenv.2014.05.114
[10] Gilani R A, Rafique M, Rehman A, et al. Biodegradation of chlorpyrifos by bacterial genus Pseudomonas[J]. Journal of Basic Microbiology, 2016, 56(2): 105−119. doi: 10.1002/jobm.201500336
[11] Zhao H, Tao K, Zhu J, et al. Bioremediation potential of glyphosate-degrading Pseudomonas spp. strains isolated from contaminated soil[J]. Journal of General & Applied Microbiology, 2015, 61(5): 165−170.
[12] Gautam P, Dubey S K. Biodegradation of imidacloprid: molecular and kinetic analysis [J/OL]. Bioresource Technology, 2022, 350: 126915[2022−04−27]. https://doi.org/10.1016/j.biortech.2022.126915.
[13] Qi Z, Wei Z. Microbial flora analysis for the degradation of beta-cypermethrin[J]. Environmental Science and Pollution Research, 2017, 24(7): 6554−6562. doi: 10.1007/s11356-017-8370-5
[14] Pang S, Lin Z, Zhang Y, et al. Insights into the toxicity and degradation mechanisms of imidacloprid via physicochemical and microbial approaches [J/OL]. Toxics, 2020, 8(3): 65[2022−04−27]. https://doi.org/10.3390/toxics8030065.
[15] Chen S, Chang C, Deng Y, et al. Fenpropathrin biodegradation pathway in Bacillus sp. DG-02 and its potential for bioremediation of pyrethroid-contaminated soils[J]. Journal of Agricultural and Food Chemistry, 2014, 62(10): 2147−2157. doi: 10.1021/jf404908j
[16] Jin Z, Guo Q, Zhang Z, et al. Biodegradation of type Ⅱ pyrethroids and major degraded products by a newly isolated Acinetobacter sp. strain JN8[J]. Canadian Journal of Microbiology, 2014, 60(8): 541−545. doi: 10.1139/cjm-2014-0104
[17] 胡桂萍, 曹红妹, 石旭平, 等. 重金属离子对不动杆菌BCL-1降解吡虫啉的影响[J]. 生物技术通讯, 2018, 29(5): 619−624. doi: 10.3969/j.issn.1009-0002.2018.05.007 Hu G P, Cao H M, Shi X P, et al. Effect of imidacloprid degrading strain BCL-1 by heavy metal ions[J]. Letters in Biotechnology, 2018, 29(5): 619−624. doi: 10.3969/j.issn.1009-0002.2018.05.007
[18] Zhang W, Li J, Zhang Y, et al. Characterization of a novel glyphosate-degrading bacterial species, Chryseobacterium sp. Y16C, and evaluation of its effects on microbial communities in glyphosate-contaminated soil [J/OL]. Journal of Hazardous Materials, 2022, 432: 128689 [2022−04−27]. https://doi.org/10.1016/j.jhazmat.2022.128689.
[19] Qu J, Xu Y, Ai G M, et al. Novel Chryseobacterium sp. PYR2 degrades various organochlorine pesticides (OCPs) and achieves enhancing removal and complete degradation of DDT in highly contaminated soil [J/OL]. Journal of Environmental Management, 2015, 161: 350−357.
[20] Jadhav S S, David M. Biodegradation of flubendiamide by a newly isolated Chryseobacterium sp. strain SSJ1 [J/OL]. 3 Biotech, 2016, 6(1): 31[2022−04−27]. https://doi.org/10.1007/s13205-015-0347-9.
[21] Park H, Seo S I, Lim J H, et al. Screening of carbofuran-degrading bacteria Chryseobacterium sp. BSC2-3 and unveiling the change in metabolome during carbofuran degradation [J/OL]. Metabolites, 2022, 12(3): 219[2022−04−27]. https://doi.org/10.3390/metabo12030219.
[22] Silambarasan S, Abraham J. Biodegradation of carbendazim by a potent novel Chryseobacterium sp. JAS14 and plant growth promoting Aeromonas caviae JAS15 with subsequent toxicity analysis [J/OL]. 3 Biotech, 2020, 10(7): 326[2022−04−27]. https://doi.org/10.1007/s13205-020-02319-w.
[23] 姚晓华. 新杀虫剂啶虫脒对旱地土壤微生物生态影响及其降解研究 [D]. 杭州: 浙江大学, 2005. Yao X H. Effects of new pesticide acetamiprid on microbial ecology in upland soil and degradation of acetamiprid [D]. Hangzhou: Zhejiang University, 2005.
[24] Baćmaga M, Wyszkowska J, Kucharski J. The influence of chlorothalonil on the activity of soil microorganisms and enzymes[J]. Ecotoxicology, 2018, 27(9): 1188−1202. doi: 10.1007/s10646-018-1968-7
[25] Chen X M, Wang X Y, Lu W, et al. Use of Beauveria bassiana in combination with commercial insecticides to manage Phauda flammans (Walker) (Lepidoptera: Phaudidae): testing for compatibility and synergy[J]. Journal of Asia-Pacific Entomology, 2021, 24(2): 272−278. doi: 10.1016/j.aspen.2021.01.016
[26] Luo Y, Yang R, Li Y, et al. Accumulation and fate processes of organochlorine pesticides (OCPs) in soil profiles in Mt. Shergyla, Tibetan Plateau: a comparison on different forest types[J]. Chemosphere, 2019, 231: 571−578. doi: 10.1016/j.chemosphere.2019.05.181
[27] Kylin H, Svensson T, Jensen S, et al. The trans-continental distributions of pentachlorophenol and pentachloroanisole in pine needles indicate separate origins [J]. Enviromental Pollution, 229: 688−695.
[28] 卢虎, 姚拓, 李建宏,等. 高寒地区不同退化草地植被和土壤微生物特性及其相关性研究[J]. 草业学报, 2015, 24(5): 34−43. doi: 10.11686/cyxb20150505 Lu H, Yao T, Li J H, et al. Vegetation and soil microorganism characteristics of degraded grasslands[J]. Acta Prataculturae Sinica, 2015, 24(5): 34−43. doi: 10.11686/cyxb20150505
[29] 钱存柔, 黄怡秀. 微生物学实验教程 [M]. 北京: 北京大学出版社, 1999: 16−81. Qian C R, Huang Y X. Laboratory experiments in microbiology [M]. Beijing: Peking University Press, 1999: 16−81.
[30] 王晗, 严占勇, 张定贵, 等. 一种土壤中烟草疫霉菌的快速分离鉴定及计数方法[J]. 中国农学通报, 2012, 28(9): 163−168. doi: 10.3969/j.issn.1000-6850.2012.09.032 Wang H, Yan Z Y, Zhang D G, et al. A fast method of isolation, identification and counting of Phytophthora nicotianae from soil[J]. Chinese Agricultural Science Bulletin, 2012, 28(9): 163−168. doi: 10.3969/j.issn.1000-6850.2012.09.032
[31] 东秀珠, 蔡妙英. 常见细菌系统鉴定手册[M]. 北京: 科学出版社, 2001: 349−418. Dong X Z, Cai M Y. Handbook for the identification of common bacterial systems[M]. Beijing: Science Press, 2001: 349−418.
[32] Buchanan R E, Gibbons N E. 伯杰细菌鉴定手册[M]. 北京: 科学出版社, 1984: 16−1207. Buchanan R E, Gibbons N E. Bergey’s manual of determinative bacteriology[M]. Beijing: Science Press, 1984: 16−1207.
[33] 谢家仪, 董光军, 刘振英. 扫描电镜的微生物样品制备方法[J]. 电子显微学报, 2005(4): 440. doi: 10.3969/j.issn.1000-6281.2005.04.191 Xie J Y, Dong G J, Liu Z Y. Preparation of microbial samples by scanning electron microscopy[J]. Journal of Chinese Electron Microscopy Society, 2005(4): 440. doi: 10.3969/j.issn.1000-6281.2005.04.191
[34] 宋超, 周杨全, 李义强, 等. 三种新烟碱类杀虫剂在土壤中的残留降解及影响因子[J]. 农药学学报, 2016, 18(6): 738−744. doi: 10.16801/j.issn.1008-7303.2016.0104 Song C, Zhou Y Q, Li Y Q, et al. Residue degradation and influencing factors of three neonicotinoids insecticides in soil[J]. Chinese Journal of Pesticide Science, 2016, 18(6): 738−744. doi: 10.16801/j.issn.1008-7303.2016.0104
[35] 郭晓青, 王秀娟, 孙爱丽, 等. 环境中拟除虫菊酯类农药微生物降解技术研究进展[J]. 中国生物工程杂志, 2017, 37(5): 126−132. Guo X Q, Wang X J, Sun A L, et al. Advances of studies on microbial degradation of pyrethroid insecticides[J]. China Biotechnology, 2017, 37(5): 126−132.
[36] 景岳龙. 拟除虫菊酯降解菌的筛选、鉴定及降解性能研究[D]. 杨凌: 西北农林科技大学, 2010. Jing Y L. Isolation and identification of degradation bacteria for synthetic pyrethroids and its degradation characteristics[D]. Yangling: Northwest A&F University, 2010.
[37] 聂司宇, 孟昊, 王淑红. 微生物对有机磷农药残留的降解[J]. 环境保护与循环经济, 2020, 40(3): 44−49. doi: 10.3969/j.issn.1674-1021.2020.03.012 Nie S Y, Meng H, Wang S H. Degradation of organophosphorus pesticide residues by microorganisms[J]. Environmental Protection and Circular Economy, 2020, 40(3): 44−49. doi: 10.3969/j.issn.1674-1021.2020.03.012
[38] Siripattanakul-Ratpukdi S, Vangnai A S, Sangthean P, et al. Profenofos insecticide degradation by novel microbial consortium and isolates enriched from contaminated chili farm soil[J]. Environmental Science and Pollution Research International, 2015, 22(1): 320−328. doi: 10.1007/s11356-014-3354-1
[39] 马青云, 江旭, 李情情, 等. 烟嘧磺隆降解菌Chryseobacterium sp. LAM-M5的分离, 鉴定及其降解机理研究[J]. 生物技术通报, 2022, 38(2): 113−122. Ma Q Y, Jiang X, Li Q Q, et al. Isolation and identification of nicosulfuron degrading strain Chryseobacterium sp. LAM-M5 and study on its degradation pathway[J]. Biotechnology Bulletin, 2022, 38(2): 113−122.
[40] 于晓菲, 夏清风, 金朝霞. 高效氯氰菊酯降解菌的筛选及其降解特性[J]. 大连工业大学学报, 2013, 32(6): 417−421. doi: 10.19670/j.cnki.dlgydxxb.2013.06.007 Yu X F, Xia Q F, Jin Z X. Isolation of beta-cypermethrin degrading bacterium and its degradation characteristics[J]. Journal of Dalian Polytechnic University, 2013, 32(6): 417−421. doi: 10.19670/j.cnki.dlgydxxb.2013.06.007
[41] 林启美, 赵小蓉, 孙焱鑫, 等. 四种不同生态系统的土壤解磷细菌数量及种群分布[J]. 土壤与环境, 2000, 9(1): 34−37. Lin Q M, Zhao X R, Sun Y X, et al. Community characters of soil phosphobacteria in four ecosystems[J]. Ecology and Environmental Sciences, 2000, 9(1): 34−37.
[42] 张爱民, 李乃康, 赵钢勇, 等. 土壤中解磷、解钾微生物研究进展[J]. 河北大学学报(自然科学版), 2015, 35(4): 442−448. Zhang A M, Li N K, Zhao G Y, et al. Research progress on the phosphate-solubilizing and potassium-solubilizing microorganisms[J]. Journal of Hebei University (Natural Science Edition), 2015, 35(4): 442−448.
[43] 刘亚冬. 玉米种衣剂中的农药在土壤中的残留及对细菌和酶活性的影响[D]. 重庆: 西南大学, 2021. Liu Y D. Residues of pesticides in corn seed treatment and their effects on bacteria and enzyme activities in soil[D]. Chongqing: Southwest University, 2021.
[44] 何微, 朱捷, 岳苑, 等. 宁夏枸杞种植地土壤中微生物分布调查及降解农残研究[J]. 安全与环境学报, 2022, 22(1): 360−370. doi: 10.13637/j.issn.1009-6094.2021.0096 He W, Zhu J, Yue Y, et al. Study on the distribution of soil microorganisms and degradation of pesticide residue in Ningxia Lycium field[J]. Journal of Safety and Environment, 2022, 22(1): 360−370. doi: 10.13637/j.issn.1009-6094.2021.0096
[45] 刘曼, 辛颖, 赵雨森. 氯氟氰菊酯对水源涵养林土壤微生物及酶活性的影响[J]. 东北林业大学学报, 2013, 41(6): 80−83. doi: 10.3969/j.issn.1000-5382.2013.06.019 Liu M, Xin Y, Zhao Y S. Effect of cyhalothrin on soil microorganism and enzyme activity of water conservation forest[J]. Journal of Northeast Forestry University, 2013, 41(6): 80−83. doi: 10.3969/j.issn.1000-5382.2013.06.019
[46] 史婕, 申鸿, 郭涛, 等. 氯氰菊酯对紫色土土著微生物数量及土壤酶活性的影响[J]. 西南大学学报(自然科学版), 2012, 34(5): 97−101. Shi J, Shen H, Guo T, et al. Effect of cypermethrin on the indigenous microorganism quantity and enzyme activity of the purplish soil[J]. Journal of Southwest University (Natural Science Edition), 2012, 34(5): 97−101.
[47] 张清明, 冯瑞芝, 张保华, 等. 盐胁迫下吡虫啉对棉田土壤微生物数量及酶活性的影响[J]. 水土保持研究, 2014, 21(3): 25−30. doi: 10.13869/j.cnki.rswc.2014.03.006 Zhang Q M, Feng R Z, Zhang B H, et al. Effects of imidacloprid on soil microbes and enzyme activities under the salinity stress[J]. Research of Soil and Water Conservation, 2014, 21(3): 25−30. doi: 10.13869/j.cnki.rswc.2014.03.006
[48] 沙月霞. 吡虫啉对枸杞土壤微生物群落功能多样性的影响[J]. 西北农业学报, 2015, 24(9): 119−126. doi: 10.7606/j.issn.1004-1389.2015.09.018 Sha Y X. Effects of imidacloprid application on diversity of microbial community function in Lycium barbarum soil[J]. Acta Agriculturae Boreali-Occidentalis Sinica, 2015, 24(9): 119−126. doi: 10.7606/j.issn.1004-1389.2015.09.018
-
期刊类型引用(0)
其他类型引用(2)



 下载:
下载: