Characteristics of soil microbial community structure with different plantation ages in larch forest in Taiyue Mountain of Shanxi Province, northern China
-
摘要:目的 分析不同林龄华北落叶松人工林土壤微生物结构特征变化规律,阐明土壤微生物群落结构特征对林龄变化的响应机制及关键影响因子,为人工林可持续经营和探讨土壤微生物群落对环境变化反馈机制提供理论依据。方法 以不同林龄华北落叶松人工林为研究对象,基于土壤微生物群落结构、土壤理化性质和林下植被特征等指标,采用冗余分析探讨土壤理化性质和林下植被特征对土壤微生物群落结构的驱动机制。结果 研究结果表明林龄变化对土壤理化性质和微生物群落结构特征均存在显著影响,其中土壤温度、含水率、pH值、全碳、全氮、全磷、铵态氮和硝态氮含量均随着人工林年龄的增加而显著增加,土壤有效磷含量则表现出相反的变化规律(P < 0.05)。林龄增长也提高了土壤革兰氏阳性细菌、革兰氏阴性细菌、真菌和放线菌含量,但真菌与细菌以及革兰氏阳性细菌与革兰氏阴性细菌的比值呈下降趋势。林下灌木、草本层物种多样性也表现出随林龄增加而增长的变化趋势,不同林龄间差异则均未达显著水平。冗余分析结果表明本研究选取的土壤理化性质和林下植物物种多样性指标共同解释了土壤微生物群落总变异的86.1%,土壤含水率、温度、有效磷、硝态氮含量、灌木层丰富度指数和草本层丰富度指数则分别解释了微生物群落结构变异程度的22.7%、18.4%、11.8%、10.6%、7.9%和5.6%。结论 土壤微生物群落结构特征、土壤理化性质和林下植物物种多样性(灌木层和草本层)均受到林龄变化的影响,并且土壤温度、含水率、有效磷、硝态氮和林下植物物种多样性是引起不同林龄人工林土壤微生物群落结构变化的关键驱动因子。Abstract:Objective This paper aims to analyze the variation of soil microbial community structure characteristics of larch plantation at different plantation ages, clarify the response mechanism of soil microbial community structure to the changes of plantation age and its key influencing factors, provide theoretical basis for sustainable management of the plantation and feedback effect of soil microbial community to environmental changes.Method Based on the characteristics of soil microbial community structure, soil physical and chemical properties and understory vegetation characteristics database, this study explored the regulation mechanism of soil physical and chemical properties and understory vegetation characteristics on the formation of soil microbial communities by redundancy analysis.Result The change of plantation age had a significant impact on soil physical and chemical properties and microbial community structure, such as soil temperature, water content, pH, total carbon, total nitrogen, total phosphorus, ammonium nitrogen and nitrate nitrogen content increased significantly with the increase of plantation age, but the soil available phosphorus content showed the opposite trend (P < 0.05). Meanwhile, the growth of the plantation age also significantly increased the abundance of gram-positive bacteria, gram-negative bacteria, fungi and actinomycetes in the soil, while the ratio of fungi: bacteria and gram-positive bacteria: gram-negative bacteria showed a downward trend. The diversity of understory shrubs and herb layers also showed a trend of increasing with the increase of forest age, and the differences between different forest ages did not reach a significant level. The results of redundant analysis showed that the soil physical and chemical properties and the understory vegetation diversity index explained 86.1% of the total variation of the soil microbial community, while the soil water content, soil temperature, available phosphorus, nitrate nitrogen content, and the richness index of shrub and herb layer explained 22.7%, 18.4%, 11.8%, 10.6%, 7.9% and 5.6% of the variation of microbial community structure, respectively.Conclusion The structural characteristics of soil microbial community, soil physical and chemical properties, and understory plant diversity (ie shrub layer and herb layer) are all affected by changes of plantation age. Notably, soil temperature, water content, available phosphorus, nitrate nitrogen, and understory vegetation diversity are key factors to drive the changes of soil microbial community structure in different plantation ages.
-
土壤微生物作为森林生态系统中最活跃生命组分之一,是地球化学循环的关键环节,在有机质分解、养分元素循环和土壤肥力维持等方面有着重要的作用[1-4]。因此,土壤微生物被认为是评价土壤质量和指示生产力的重要指标。土壤微生物群落对土壤微环境因子变化十分敏感,往往能对土壤水热条件和养分元素浓度等因素的改变迅速做出反应,从而引起微生物群落结构的变化[5-8]。在森林生态系统中,地上植被多样性的变化被认为是影响土壤微生物群落结构的重要因素之一[9-12],不仅可通过改变地上植物生物量、凋落叶和细根数量、组成和分解速率等来直接影响土壤微生物群落[13-15],还可通过影响土壤水热条件、养分元素含量和林下微气候等因子间接影响微生物群落结构[16-18]。关于环境因子对人工林土壤微生物群落调控机制的研究受到越来越多生态学家的关注。
华北落叶松(Larix principis-rupprechtii)是中国北方造林的重要树种之一,在木材生产、水土保持和固碳释氧等方面发挥重要作用[19]。然而,由于不合理经营管理措施引起了诸如土壤肥力退化、人工林养分循环效率低下、林下植物多样性较差等一系列生态问题[20-22]。虽然近年来针对华北落叶松人工林展开了一系列的研究,但多数研究主要集中在土壤肥力、人工林生产力和林地生物多样性等方面[23-25],关于土壤微生物群落结构对林龄梯度变化的响应机制及关键影响因子的研究相对较少。因此,本文以太岳山不同林龄华北落叶松人工林为研究对象,通过磷脂脂肪酸(phospholipid fatty acids,PLFA)法分析其土壤微生物群落结构变化特征,探讨林下植被和土壤理化性质对土壤微生物群落驱动机制,以期进一步了解太岳山不同林龄华北落叶松林土壤微生物群落结构特征和生态功能,为该地区林地资源的可持续经营提供科学的理论依据和实践指导。
1. 研究区概况与研究方法
1.1 研究区概况
本研究位于山西省长治市沁源县好地方林场(36°40′N、112°05′E),该地区年平均气温约为6.1 ℃,最高温在夏季7月份,约为15 ℃,最低温在12月末至1月初,约为−11 ℃。年降雨量为700 mm左右,雨季约从当年5月持续至9月,但降水期多集中于6—8月份。全年无霜期仅有125 d左右,其生长季从4月末5月初持续至10月中上旬。该地区森林类型主要涵盖针叶林、针阔混交林和阔叶林,其中针叶林是该地区森林的主要类型。本项研究选取的华北落叶松人工林样地分别为Lar30、Lar40和Lar50,其中Lar50华北落叶松人工林(林龄为53年)主要在20世纪70年代左右种植,Lar40华北落叶松人工林(林龄为42年)主要在20世纪80年代初种植,Lar30华北落叶松人工林(林龄为33年)是在20世纪90年代初期种植的。栽植所选取的苗木为生长良好,基径超过0.6 cm,苗高在25 cm以上的2年生苗,完成生根粉浸根处理后在山区沿等高线进行栽植。林下主要灌木植物有绣线菊(Spiraea salicifolia)、黄刺玫(Rosa xanthine)和胡枝子(Lespedeza bicolor)等;草本植物主要有唐松草(Thalictrum aquilegiifolium var. sibiricum)、糙苏(Phlomis umbrosa)和玉竹(Polygonatum odoratum)等。
1.2 样地设置和土壤样品采集
2014年7月,以Lar30、Lar40和Lar50华北落叶松人工林群落为研究对象,共设置12块20 m × 30 m的固定样地进行人工林基础信息的采集和记录,包括样地坡向、坡度、海拔、林分密度、林下植被等信息(表1)。林下灌木层和草本层香农多样性指数、丰富度指数和均匀度指数的计算按照Dang等[5]的方法进行。2018年8月份在不同林龄人工林各样地中通过S型采样法对0~10 cm土层进行9点采样。在去除土壤中明显凋落物、石砾和植物残体等杂物后对鲜土进行过筛(土筛孔径为2 mm)并分为2份尽快装入保温箱送回实验室进行相关指标测定。
表 1 不同林龄华北落叶松人工林样地基本情况Table 1. Basic situation of larch plantation sample plots with different forest ages项目
Item林龄梯度 Plantation age gradient Lar30 Lar40 Lar50 林龄/a Stand age
/year33 42 53 坡度 Slope
/(°)25 25 25 坡向
Aspect东南 Southeast 东南 Southeast 东南 Southeast 平均树高 Mean tree height
/m16.3 ± 0.8 18.8 ± 1.3 16.1 ± 1.4 平均胸径 Mean DBH
/cm16.4 ± 0.5 18.7 ± 1.6 22.6 ± 2.8 郁闭度
Canopy density0.28 ± 0.02 0.35 ± 0.01 0.39 ± 0.01 林分密度/(株·hm−2)
Plantation density/(tree·ha−1)1158 ± 87 1341 ± 62 803 ± 24 凋落物层生物量/(t·hm−2) Biomass of litter layer/(t·ha−1) 43.2 ± 10.8 106.9 ± 18.3 50.9 ± 8.2 注:Lar30.林龄33年人工林;Lar40.林龄42年人工林;Lar50.林龄53年人工林。下同。Notes: Lar30, 33-year-old plantation; Lar40, 42-year-old plantation; Lar50, 53-year-old plantation. The same below. 1.3 土壤理化性质测定
将带回实验室土壤中的一份进行自然风干、研磨并根据待测定指标的实验标准进行筛分,另一部分土壤则存入0 ~ 4 ℃条件的冰箱中保存待用。土壤有机碳含量通过重铬酸钾外加热法进行测定[26];土壤全氮和全磷分别采样浓硫酸−混合加速剂消化法和浓硫酸−高氯酸消化法对土样进行消化处理后[26],在连续流动分析仪器上(AA3,SEAL Analytical GmbH,Germany)测定。土壤铵态氮、硝态氮的测定首先称取10 g已经过2 mm土筛的新鲜土样于250 mL广口瓶中,加入1 mol/L氯化钾溶液100 mL,塞紧瓶塞后经过振荡器震荡1 h以上[26]。将浸提液过滤后采用连续流动分析仪器分析土壤铵态氮和硝态氮含量。土壤有效磷含量测定步骤为称取5 g土样并加入0.5 mol/L碳酸氢钠溶液振荡1 h以上,而后将浸提液用无磷滤纸过滤[26],最后通过连续流动分析仪器进行有效磷含量测定[26]。
土壤pH值使用pH计(Five Easy,Mettler-Toledo,Switzerland)测定[26],土壤水分含量的测定则是采用烘干法测定烘干10 g新鲜土样至恒质量后的质量损失来计算土壤水分含量[26]。土壤温度则在采集土样时通过土壤温度测定仪(Li-COR Biosciences,Lincoln,NE,USA)进行测定。
1.4 土壤微生物群落结构
通过PLFA方法对不同林龄土壤微生物群落结构进行测定,主要过程包括从土样中提取脂质、采样碱性甲醇分解并回收甲酯化的脂肪酸样品。而后根据已知含量的甲酯(19∶0)作为内标测定PLFAs含量。其中,革兰氏阳性菌选择 i13∶0,i14∶0,a14∶0,a15∶0,i15∶0,i16∶0,a17∶0,i17∶0,i18∶0 表征[27-28];革兰氏阴性菌选择 10∶0 2OH,15∶1 w4c,15∶1 w6c,16∶0 2OH,16∶1 w6c,16∶1 w7c,16∶1 w9c,cy17∶0,17∶1 w8c,18∶1 w5c,18∶1 w7c, cy19∶0 表征[27, 29-30],真菌选择 16∶1 w5c,18∶1 w9c,18∶2 w6c,18∶2 w9c表征[27, 30-31];放线菌选择 10 Me 16∶0,10 Me 17∶0,10 Me 18∶0表征[31-32]。
1.5 数据处理
采用Microsoft Office Excel 2011软件对相关数据进行初步录入,使用统计软件 SPSS 20.0 对数据进行描述性统计分析和方差分析等,RDA分析在Canoco Software 5. 0中进行,图表绘制通过Sigmaplot 12.0 进行。
2. 结果与分析
2.1 土壤理化性质
土壤pH值变化范围在6.28 ~ 6.56之间,且随着林龄增加表现出逐步上升的变化趋势,特别是Lar50人工林中的土壤pH值相对较高,但不同林龄间土壤pH值差异未达显著水平(P > 0.05)。Lar40和Lar50人工林中土壤含水率均显著高于Lar30人工林(P < 0.05)。土壤温度则随着林龄的增加呈逐步上升的变化趋势,且在Lar50林分中达到峰值。土壤有机碳、全氮、铵态氮和硝态氮含量均在Lar50人工林中显著高于Lar30(P < 0.05),土壤全磷含量在Lar40和Lar50人工林中显著高于Lar30(P < 0.05),但土壤有效磷含量在Lar50人工林中则显著低于Lar30和Lar40(P < 0.05)(表2)。
表 2 不同林龄华北落叶松人工林土壤理化性质Table 2. Soil physicochemical properties of larch plantations with different forest ages土壤理化性质
Soil physical and chemical property林龄梯度
Plantation age gradientLar30 Lar40 Lar50 pH值
pH value6.28 ± 0.09a 6.35 ± 0.11a 6.56 ± 0.08a 含水率
Water content/%51.34 ± 2.54a 60.18 ± 5.16b 65.49 ± 3.78c 温度
Temperature/℃10.95 ± 0.87a 11.75 ± 0.29ab 13.45 ± 0.92b 有机碳
Organic carbon/(g·kg−1)25.12 ± 1.67a 26.88 ± 2.04ab 30.49 ± 2.30b 全氮
Total nitrogen/(g·kg−1)3.84 ± 0.21a 4.11 ± 0.26b 4.39 ± 0.17c 全磷
Total phosphorus/(g·kg−1)0.46 ± 0.02a 0.71 ± 0.11b 0.74 ± 0.03b 硝态氮
Nitrate nitrogen/(mg·kg−1)9.37 ± 1.13a 10.28 ± 0.56ab 12.94 ± 1.86b 铵态氮
Ammonium nitrogen/(mg·kg−1)3.97 ± 0.24a 4.38 ± 0.31b 5.16 ± 0.57c 有效磷
Available phosphorus/(mg·kg−1)4.98 ± 0.07a 4.92 ± 0.39a 4.56 ± 0.28b 注:不同字母表示在不同林龄间存在显著差异(P < 0.05)。Note: different letters mean significant differences among 3 plantation ages (P < 0.05). 2.2 林下植物物种多样性
由表3可知,华北落叶松人工林草本层香农多样性指数、丰富度指数和均匀度指数在Lar40和Lar50人工林中相对较高。灌木层香农多样性指数、丰富度指数和均匀度指数也在Lar50人工林中较高,其次依次为Lar40和Lar30。但总体上看,林龄增长虽然对华北落叶松人工林林下植物物种多样性存在一定促进作用但均未达显著差异水平(P > 0.05)。
表 3 不同林龄林下植物物种多样性Table 3. Species diversity of understory plants at different forest ages林龄梯度
Plantation age gradient草本层多样性
Herb layer diversity灌木层多样性
Diversity of shrub layer香农多样性指数
Shannon index丰富度指数
Richness index均匀度指数
Evenness index香农多样性指数
Shannon index丰富度指数
Richness index均匀度指数
Evenness indexLar30 3.18 ± 0.19a 25.67 ± 4.04a 0.90 ± 0.01a 1.60 ± 0.06a 6.33 ± 2.08a 0.90 ± 0.01a Lar40 3.21 ± 0.10a 28.33 ± 3.51a 0.92 ± 0.02a 1.74 ± 0.08a 6.67 ± 1.53a 0.91 ± 0.02a Lar50 3.23 ± 0.25a 30.67 ± 3.79a 0.94 ± 0.01a 1.83 ± 0.33a 7.00 ± 2.00a 0.91 ± 0.02a 注:不同字母表示各指标在不同林龄处理间存在显著差异(P < 0.05)。Note: different letters indicate that there are significant differences among varied forest age treatments (P < 0.05). 2.3 土壤微生物群落结构
如表4所示:不同林龄对土壤革兰氏阳性细菌、革兰氏阴性细菌、真菌和放线菌含量存在不同程度的影响。具体而言:在不同林龄华北落叶松人工林中,土壤革兰氏阳性细菌含量为4.39 ~ 6.37 nmol/g,Lar50和Lar40林分比Lar30分别高28.02%和45.10%;土壤革兰氏阴性细菌含量为3.52 ~ 4.84 nmol/g,Lar50和Lar40林分比Lar30分别高20.74%和37.50%;土壤放线菌含量为1.60 ~ 2.12 nmol/g,Lar50和Lar40林分比Lar30分别高11.88%和32.50%。土壤真菌含量为0.74 ~ 0.80 nmol/g,但各林龄间差异性未达显著水平。此外,本研究还比较了不同林龄华北落叶松人工林土壤微生物群落革兰氏阳性细菌与革兰氏阴性细菌比以及真菌与细菌比。二者在不同林龄间从高到低依次均为Lar30 > Lar50 > Lar40。
表 4 不同林龄土壤微生物群落特征Table 4. Characteristics of soil microbial community in different forest agesPLFA生物量
PLFA biomass林龄梯度
Plantation age gradientLar30 Lar40 Lar50 革兰氏阳性细菌 Gram-positive bacteria (G+)/(nmol·g−1) 4.39 ± 1.34a 5.62 ± 1.25b 6.37 ± 1.04c 革兰氏阴性细菌 Gram-negative bacteria (G−)/(nmol·g−1) 3.52 ± 1.06a 4.25 ± 1.46b 4.84 ± 1.20c 真菌 Fungi (F)/
(nmol·g−1)0.74 ± 0.08a 0.78 ± 0.03a 0.80 ± 0.04a 放线菌 Actinmycete (ACT)/
(nmol·g−1)1.60 ± 0.25a 1.79 ± 0.46b 2.12 ± 0.34c 革兰氏阳性细菌∶革兰氏阴性细菌 Gram-positive bacteria ∶ Gram-negative bacteria (G+∶G−) 1.42 ± 0.18a 1.26 ± 0.27a 1.39 ± 0.21a 真菌∶细菌
Fungi ∶ bacteria (F∶B)0.11 ± 0.01a 0.08 ± 0.02a 0.09 ± 0.01a 注:不同字母表示不同林龄间存在显著差异(P < 0.05)。Note: different letters indicate significant differences among varied forest ages (P < 0.05). 2.4 不同林龄对土壤微生物群落结构关键影响因子分析
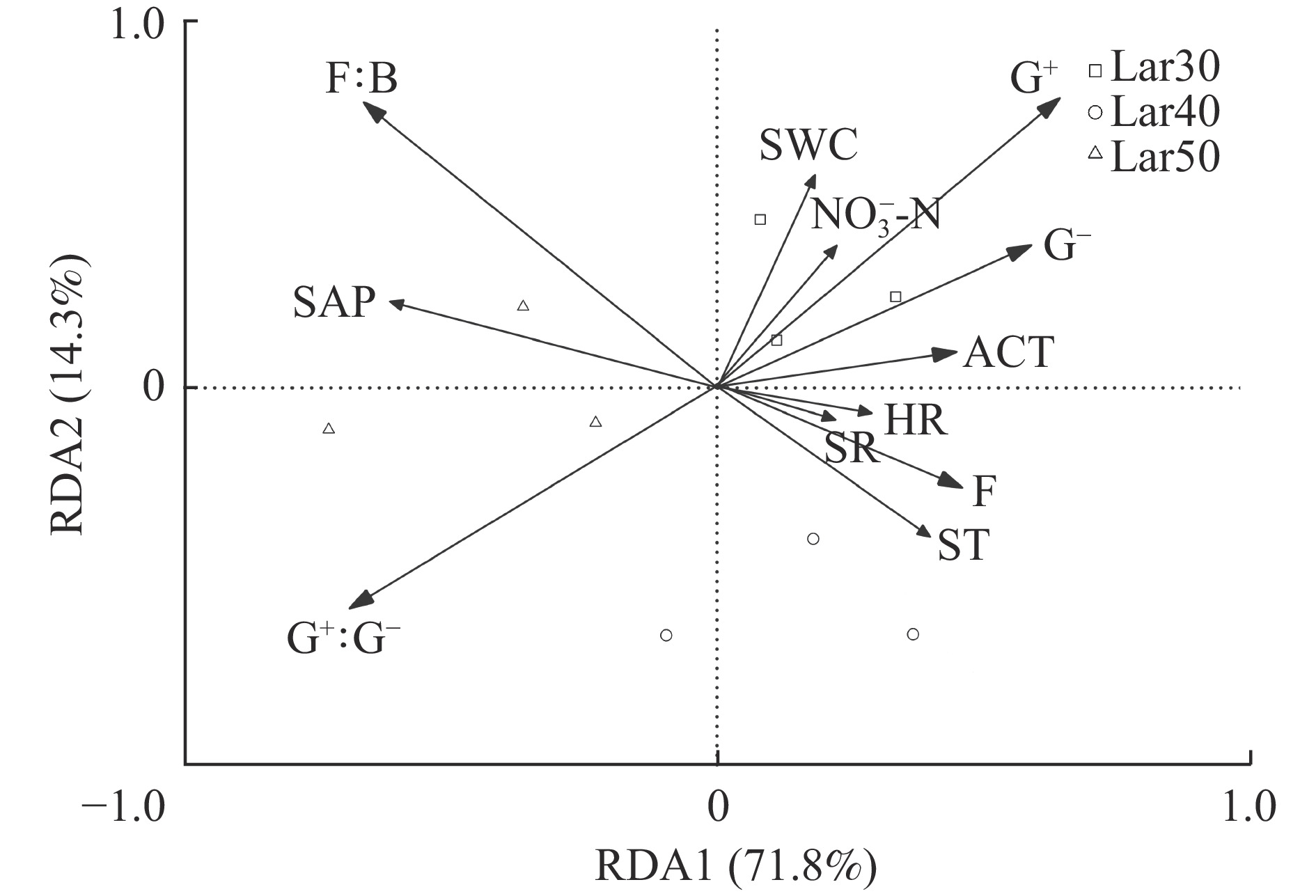
经过置换检验筛选后采用RDA分析,探讨影响土壤微生物群落结构的关键影响因子。由图1可知土壤pH值、含水率、温度、养分元素含量和林下植物物种多样性对微生物群落结构的影响,结果表明:Lar30、Lar40和Lar50林分间土壤微生物群落明显分开,说明林龄增长导致林地土壤微生物群落结构出现明显变化;第1轴和第2轴的特征值分别为0.718和0.143,即共同解释了土壤微生物群落总变异的86.1%。土壤有效磷含量与第1轴呈负相关,土壤含水率、温度、硝态氮含量、灌木层丰富度指数和草本层丰富度指数与第1轴呈正相关,分别解释了微生物群落结构变异程度的11.8%、22.7%、18.4%、10.6%、7.9%和5.6%,这说明土壤含水率、温度、有效磷含量、硝态氮含量、灌木层和草本层丰富度指数是不同林龄人工林表层土壤中微生物群落结构变化的主要影响因子。
![]() 图 1 土壤微生物群落结构影响的冗余分析ST. 土壤温度;SWC. 土壤含水率;SAP. 土壤有效磷;NO3−-N. 土壤硝态氮;SR. 灌木层物种丰富度指数;HR. 草本层物种丰富度指数。ST, soil temperature; SWC, soil water content; SAP, soil available phosphorus; NO3−-N, nitrate nitrogen; SR, richness index of shrub; HR, richness index of herb.Figure 1. Redundancy analysis of relationships of soil microbial community structure to soil factors and understory vegetation diversity
图 1 土壤微生物群落结构影响的冗余分析ST. 土壤温度;SWC. 土壤含水率;SAP. 土壤有效磷;NO3−-N. 土壤硝态氮;SR. 灌木层物种丰富度指数;HR. 草本层物种丰富度指数。ST, soil temperature; SWC, soil water content; SAP, soil available phosphorus; NO3−-N, nitrate nitrogen; SR, richness index of shrub; HR, richness index of herb.Figure 1. Redundancy analysis of relationships of soil microbial community structure to soil factors and understory vegetation diversity3. 讨 论
3.1 林龄对土壤理化性质和林下植物物种多样性影响
土壤作为森林生态系统的重要组成部分,pH值、含水率、温度和养分元素含量等理化性质对人工林中植物生长具有重要作用[15, 22]。前人研究指出林龄变化可以通过影响地上植被对土壤养分利用效率来影响土壤养分浓度[25],同时林分群落结构和物种多样性的差异等也会间接改变诸如透光率、穿透雨量、凋落物产量等林下微环境因素,从而促进土壤养分含量的积累,提高土壤养分水平[6, 17, 33]。在本研究中,Lar50和Lar40林地土壤pH值、含水率、温度和养分元素浓度总体上高于Lar30,表明林龄的增加可能更有利于提高土壤物理性质和促进土壤养分含量积累,这与罗达等[2]和Chen等[34]等在云杉(Picea asperata)人工林和油松(Pinus tabuliformis)人工林中进行的研究结果相似。此外,本研究结果还表明土壤有效磷含量在Lar30和Lar40林地土壤中显著高于Lar50,这可能是由于地上植被对土壤有效磷的需求随林龄增长而增加,从而不利于土壤有效磷含量的积累,因此在Lar50华北落叶松人工林中出现磷缺乏现象,应通过合理施用磷肥以保证林木生长对磷素的需求。
在本研究中,随着人工林林龄增加,林下灌木层和草本层物种多样性总体也呈上升趋势(表3)。通常在人工林幼龄或中龄阶段,林下植被尚处于发展阶段,灌木层和草本层各物种间存在剧烈养分竞争和排斥现象,从而导致林下物种多样性下降[25, 33];随着林龄增加,林分结构逐步趋于稳定,此时各种适应人工林环境的灌木层和草本层物种逐渐共存,林下物种多样性也相对较高[7, 25, 33]。
3.2 土壤理化性质和林下植被对土壤微生物结构的影响
本研究结果表明林龄增加能有效提高人工林土壤中革兰氏阳性细菌、革兰氏阴性细菌和放线菌含量,同时土壤理化性质、灌木层和草本层物种丰富度指数是驱动不同林龄人工林土壤微生物群落结构变化的主要因素。Chen等[34]和Liu等[35]等研究认为,林龄的增长往往有利于提高地上植被生物量、改善土壤水热环境和提高土壤养分水平,从而增加土壤微生物活性,进而提高土壤微生物生物量;且随着林龄的增加,地表凋落物数量、地下细根生物量及其分解效率等均会发生变化,这可能会加快养分元素归还效率并影响土壤中微生物群落结构和各菌群含量,这与本文研究结果相似。Fu等[36]研究提出人工林乔木层物种相对简单,林下植被多样性的变化可能与土壤微生物群落间关系更为密切。多数研究结果也提出林下植物多样性增加会丰富凋落物和细根的组成和质量,且与乔木相比,灌、草凋落叶和细根生物量对微生物群落PLFA含量影响更大,进而促进土壤微生物生物量的积累。此外,林下植被多样性还与根系分泌物数量密切相关,土壤微生物诸如细菌、真菌和放线菌等菌群的活性也受到根系分泌物的影响[33, 37]。本文研究结果也发现不同林龄人工林灌木层和草本层丰富度指数也与土壤微生物群落结构密切相关,这与Fu等[36]研究得出结论相似。
林龄增加总体上提高了土壤微生物菌群丰度,但针对不同林龄人工林土壤真菌与细菌比值和革兰氏阳性细菌与革兰氏阴性细菌比值的研究结果表明:不同林龄人工林土壤真菌与细菌比值在0.08 ~ 0.11之间,表明细菌在该地区华北落叶松人工林土壤微生物群落中占据支配地位。而不同林龄间二者比例的差异未达显著变化水平,这可能是由于与Lar30人工林相比,Lar40和Lar50人工林虽然对土壤养分元素含量存在积极的促进作用,但该地区土壤真菌群落和细菌群落总体上受营养胁迫的程度较小,林龄增长对细菌群落促进作用尽管相对高于真菌,但总体并未对土壤真菌丰度和细菌丰度产生显著影响。不同林龄人工林土壤革兰氏阳性细菌与革兰氏阴性细菌比值则在1.26 ~ 1.42之间,其中Lar50人工林土壤革兰氏阳性细菌与革兰氏阴性细菌比相对高于其余两种人工林,表明在细菌群落中,革兰氏阳性细菌是华北落叶松林土壤细菌的主要菌群。这可能是因为革兰氏阳性细菌对难分解基质利用效率相对较高,使得其在适宜的水热条件和养分情况下能够更有效的生长[1, 6, 10]。
4. 结 论
林龄增加有效改善了土壤水热状况和土壤养分含量,特别是在Lar50人工林中含水率、温度、有机碳、全氮、全磷、硝态氮、铵态氮含量均显著高于Lar30人工林,但有效磷含量则在Lar30和Lar40人工林中则相对较高。此外与Lar30人工林相比,Lar40和Lar50人工林土壤中革兰氏阳性细菌、革兰氏阴性细菌、真菌和放线菌含量较高,但真菌与细菌和革兰氏阳性细菌与革兰氏阴性细菌比值在研究区内分别为0.08 ~ 0.11和1.26 ~ 1.42之间,这表明在太岳山华北落叶松人工林群落中,土壤细菌是占据支配地位的微生物群落,同时革兰氏阳性细菌也是细菌群落中的主要菌群。土壤含水率、温度、有效磷含量、硝态氮含量、灌木层和草本层丰富度指数是不同林龄人工林土壤中微生物群落结构变化的主要影响因子,在分析土壤微生物群落影响因子时,不仅要考虑土壤水热条件和养分含量对土壤微生物群落结构的驱动作用,还需进一步分析地上植被特征对微生物群落的影响。
-
图 1 土壤微生物群落结构影响的冗余分析
ST. 土壤温度;SWC. 土壤含水率;SAP. 土壤有效磷;NO3−-N. 土壤硝态氮;SR. 灌木层物种丰富度指数;HR. 草本层物种丰富度指数。ST, soil temperature; SWC, soil water content; SAP, soil available phosphorus; NO3−-N, nitrate nitrogen; SR, richness index of shrub; HR, richness index of herb.
Figure 1. Redundancy analysis of relationships of soil microbial community structure to soil factors and understory vegetation diversity
表 1 不同林龄华北落叶松人工林样地基本情况
Table 1 Basic situation of larch plantation sample plots with different forest ages
项目
Item林龄梯度 Plantation age gradient Lar30 Lar40 Lar50 林龄/a Stand age
/year33 42 53 坡度 Slope
/(°)25 25 25 坡向
Aspect东南 Southeast 东南 Southeast 东南 Southeast 平均树高 Mean tree height
/m16.3 ± 0.8 18.8 ± 1.3 16.1 ± 1.4 平均胸径 Mean DBH
/cm16.4 ± 0.5 18.7 ± 1.6 22.6 ± 2.8 郁闭度
Canopy density0.28 ± 0.02 0.35 ± 0.01 0.39 ± 0.01 林分密度/(株·hm−2)
Plantation density/(tree·ha−1)1158 ± 87 1341 ± 62 803 ± 24 凋落物层生物量/(t·hm−2) Biomass of litter layer/(t·ha−1) 43.2 ± 10.8 106.9 ± 18.3 50.9 ± 8.2 注:Lar30.林龄33年人工林;Lar40.林龄42年人工林;Lar50.林龄53年人工林。下同。Notes: Lar30, 33-year-old plantation; Lar40, 42-year-old plantation; Lar50, 53-year-old plantation. The same below. 表 2 不同林龄华北落叶松人工林土壤理化性质
Table 2 Soil physicochemical properties of larch plantations with different forest ages
土壤理化性质
Soil physical and chemical property林龄梯度
Plantation age gradientLar30 Lar40 Lar50 pH值
pH value6.28 ± 0.09a 6.35 ± 0.11a 6.56 ± 0.08a 含水率
Water content/%51.34 ± 2.54a 60.18 ± 5.16b 65.49 ± 3.78c 温度
Temperature/℃10.95 ± 0.87a 11.75 ± 0.29ab 13.45 ± 0.92b 有机碳
Organic carbon/(g·kg−1)25.12 ± 1.67a 26.88 ± 2.04ab 30.49 ± 2.30b 全氮
Total nitrogen/(g·kg−1)3.84 ± 0.21a 4.11 ± 0.26b 4.39 ± 0.17c 全磷
Total phosphorus/(g·kg−1)0.46 ± 0.02a 0.71 ± 0.11b 0.74 ± 0.03b 硝态氮
Nitrate nitrogen/(mg·kg−1)9.37 ± 1.13a 10.28 ± 0.56ab 12.94 ± 1.86b 铵态氮
Ammonium nitrogen/(mg·kg−1)3.97 ± 0.24a 4.38 ± 0.31b 5.16 ± 0.57c 有效磷
Available phosphorus/(mg·kg−1)4.98 ± 0.07a 4.92 ± 0.39a 4.56 ± 0.28b 注:不同字母表示在不同林龄间存在显著差异(P < 0.05)。Note: different letters mean significant differences among 3 plantation ages (P < 0.05). 表 3 不同林龄林下植物物种多样性
Table 3 Species diversity of understory plants at different forest ages
林龄梯度
Plantation age gradient草本层多样性
Herb layer diversity灌木层多样性
Diversity of shrub layer香农多样性指数
Shannon index丰富度指数
Richness index均匀度指数
Evenness index香农多样性指数
Shannon index丰富度指数
Richness index均匀度指数
Evenness indexLar30 3.18 ± 0.19a 25.67 ± 4.04a 0.90 ± 0.01a 1.60 ± 0.06a 6.33 ± 2.08a 0.90 ± 0.01a Lar40 3.21 ± 0.10a 28.33 ± 3.51a 0.92 ± 0.02a 1.74 ± 0.08a 6.67 ± 1.53a 0.91 ± 0.02a Lar50 3.23 ± 0.25a 30.67 ± 3.79a 0.94 ± 0.01a 1.83 ± 0.33a 7.00 ± 2.00a 0.91 ± 0.02a 注:不同字母表示各指标在不同林龄处理间存在显著差异(P < 0.05)。Note: different letters indicate that there are significant differences among varied forest age treatments (P < 0.05). 表 4 不同林龄土壤微生物群落特征
Table 4 Characteristics of soil microbial community in different forest ages
PLFA生物量
PLFA biomass林龄梯度
Plantation age gradientLar30 Lar40 Lar50 革兰氏阳性细菌 Gram-positive bacteria (G+)/(nmol·g−1) 4.39 ± 1.34a 5.62 ± 1.25b 6.37 ± 1.04c 革兰氏阴性细菌 Gram-negative bacteria (G−)/(nmol·g−1) 3.52 ± 1.06a 4.25 ± 1.46b 4.84 ± 1.20c 真菌 Fungi (F)/
(nmol·g−1)0.74 ± 0.08a 0.78 ± 0.03a 0.80 ± 0.04a 放线菌 Actinmycete (ACT)/
(nmol·g−1)1.60 ± 0.25a 1.79 ± 0.46b 2.12 ± 0.34c 革兰氏阳性细菌∶革兰氏阴性细菌 Gram-positive bacteria ∶ Gram-negative bacteria (G+∶G−) 1.42 ± 0.18a 1.26 ± 0.27a 1.39 ± 0.21a 真菌∶细菌
Fungi ∶ bacteria (F∶B)0.11 ± 0.01a 0.08 ± 0.02a 0.09 ± 0.01a 注:不同字母表示不同林龄间存在显著差异(P < 0.05)。Note: different letters indicate significant differences among varied forest ages (P < 0.05). -
[1] 陈岳民, 高金涛, 熊德成, 等. 土壤增温对中亚热带杉木幼林土壤微生物群落结构和有效氮的影响[J]. 亚热带资源与环境学报, 2016, 11(4): 1−8. doi: 10.3969/j.issn.1673-7105.2016.04.001 Chen Y M, Gao J T, Xiong D C, et al. Effects of soil warming on soil microbial community structure and soil available nitrogen in subtropical young Chinese fir plantation[J]. Journal of Subtropical Resources and Environment, 2016, 11(4): 1−8. doi: 10.3969/j.issn.1673-7105.2016.04.001
[2] 罗达, 刘顺, 史作民, 等. 川西亚高山不同林龄云杉人工林土壤微生物群落结构[J]. 应用生态学报, 2017, 28(2): 519−527. Luo D, Liu S, Shi Z M, et al. Soil microbial community structure in Picea asperata plantations with different ages in subalpine of western Sichuan, Southwest China[J]. Chinese Journal of Ecology, 2017, 28(2): 519−527.
[3] Cui Y, Fang L, Guo X, et al. Ecoenzymatic stoichiometry and microbial nutrient limitation in rhizosphere soil in the arid area of the northern Loess Plateau, China[J]. Soil Biology & Biochemistry, 2018, 116: 11−21.
[4] Liu J, Yang Z, Peng D. Response of soil microbial community dynamics to Robinia pseudoacacia L. afforestation in the Loess Plateau: a chronosequence approach[J]. Plant and Soil, 2018, 423: 327−338. doi: 10.1007/s11104-017-3516-2
[5] Dang P, Gao Y, Liu J, et al. Effects of thinning intensity on understory vegetation and soil microbial communities of a mature Chinese pine plantation in the Loess Plateau[J]. Science of the Total Environment, 2018, 630: 171−180. doi: 10.1016/j.scitotenv.2018.02.197
[6] 姜懿珊, 肖静, 罗春玲, 等. 平顶山、长白山、赛罕乌拉森林土壤微生物群落结构分析[J]. 生态环境学报, 2014, 23(8): 1272−1279. doi: 10.3969/j.issn.1674-5906.2014.08.004 Jiang Y S, Xiao J, Luo C L, et al. The microbial community of three mountains Pingding, Changbai and Saihanwula based on the analysis of phospholipid fatty acids (PLFAs)[J]. Ecology and Environmental Sciences, 2014, 23(8): 1272−1279. doi: 10.3969/j.issn.1674-5906.2014.08.004
[7] Chen Y L, Chen L Y, Peng Y F, et al. Linking microbial C∶N∶P stoichiometry to microbial community and abiotic factors along a 3500-km grassland transect on the Tibetan Plateau[J]. Global Ecology Biogeography, 2016, 25: 1416−1427. doi: 10.1111/geb.12500
[8] Grayston S J, Prescott C E. Microbial communities in forest floors under four tree species in coastal British Columbia[J]. Soil Biology & Biochemistry, 2005, 37(6): 1157−1167.
[9] Kim S, Li G, Han S H, et al. Thinning affects microbial biomass without changing enzyme activity in the soil of Pinus densiflora Sieb. et Zucc. forests after 7 years[J]. Annals of Forest Science, 2018, 75(1): 13. doi: 10.1007/s13595-018-0690-1
[10] 杨君珑, 付晓莉, 马泽清, 等. 中亚热带5种类型森林土壤微生物群落特征[J]. 环境科学学报, 2015, 28(5): 720−727. Yang J L, Fu X L, Ma Z Q, et al. Characteristics of soil microbial community in five forest types in mid-subtropical China[J]. Research of Environmental Sciences, 2015, 28(5): 720−727.
[11] Li Q, Song X, Gu H, et al. Nitrogen deposition and management practices increase soil microbial biomass carbon but decrease diversity in Moso bamboo plantations[J]. Scientific Reports, 2016, 6: 28235. doi: 10.1038/srep28235
[12] Liu J, Sui Y, Yu Z, et al. Diversity and distribution patterns of acidobacterial communities in the black soil zone of northeast China[J]. Soil Biology & Biochemistry, 2016, 95: 212−222.
[13] Qiu X C, Peng D L, Wang H B, et al. Minimum data set for evaluation of stand density effects on soil quality in Larix principis-rupprechtii plantations in North China[J]. Ecological Indicators, 2019, 103: 236−247. doi: 10.1016/j.ecolind.2019.04.010
[14] Yang B, Pang X, Hu B, et al. Does thinning-induced gap size result in altered soil microbial community in pine plantation in eastern Tibetan Plateau?[J]. Ecology and Evolution, 2017, 7(9): 2986−2993. doi: 10.1002/ece3.2714
[15] Ren C, Zhao F, Kang D, et al. Linkages of C∶N∶P stoichiometry and bacterial community in soil following afforestation of former farmland[J]. Forest Ecology and Management, 2016, 376: 59−66. doi: 10.1016/j.foreco.2016.06.004
[16] Sorensen P O, Templer P H, Finzi A C. Contrasting effects of winter snowpack and soil frost on growing season microbial biomass and enzyme activity in two mixed-hardwood forests[J]. Biogeochemistry, 2016, 128: 141−154. doi: 10.1007/s10533-016-0199-3
[17] 马祥庆. 人工林地力衰退研究综述[J]. 南京林业大学学报(自然科学版), 1997, 21(2): 77−82. Ma X Q. Review on the decline of plantation capacity[J]. Journal of Nanjing Forestry University (Natural Sciences), 1997, 21(2): 77−82.
[18] Urbanová M, Anajdr J, Baldrian P. Composition of fungal and bacterial communities in forest litter and soil is largely determined by dominant trees[J]. Soil Biology & Biochemistry, 2015, 84: 53−64.
[19] 王玲玲, 徐福利, 王渭玲, 等. 不同林龄华北落叶松人工林土壤肥力评价[J]. 西南林业大学学报, 2016, 35(2): 17−24. Wang L L, Xu F L, Wang W L, et al. Assessment of soil fertility in different aged Larix principis-rupprechtii plantation[J]. Journal of Southwest Forestry University, 2016, 35(2): 17−24.
[20] 周霆, 盛炜彤. 关于我国人工林可持续问题[J]. 世界林业研究, 2008, 21(3): 49−53. Zhou T, Sheng W T. On the plantation sustainability in China[J]. World Forestry Research, 2008, 21(3): 49−53.
[21] Zhang J, Li M, Zheng G. Effect of stand age on soil microbial community structure in wolfberry (Lycium barbarum L.) fields[J]. Acta Ecologica Sinica, 2017, 37(1): 10−17. doi: 10.1016/j.chnaes.2016.12.003
[22] Zhang L, Wang J, Bai Z, et al. Effects of vegetation on runoff and soil erosion on reclaimed land in an opencast coal-mine dump in a loess area[J]. Catena, 2015, 128: 44−53. doi: 10.1016/j.catena.2015.01.016
[23] Zhou L, Cai L, He Z, et al. Thinning increases understory diversity and biomass, and improves soil properties without decreasing growth of Chinese fir in southern China[J]. Environmental Science and Pollution Research, 2016, 23: 24135−24150. doi: 10.1007/s11356-016-7624-y
[24] Zhao W P, Shen W J, Li Y E, et al. Interactive effects of temperature and moisture on composition of the soil microbial community[J]. European Journal of Soil Science, 2017, 68: 909−918. doi: 10.1111/ejss.12488
[25] 巫文香. 人工纯林和混交林植物、土壤微生物多样性与生态系统功能性[D]. 南宁: 广西大学, 2019. Wu W X. Plant diversity, soil microbial diversity and ecosystem multifunction in pure and mixed plantations[D]. Nanning: Guangxi University, 2019.
[26] 国家林业局. 中华人民共和国林业行业标准−森林土壤分析方法[M]. 北京: 中国标准出版社, 2000. State Forestry Administration. Forestry industry standard of the people ’s Republic of China: forest soil analysis method[M]. Beijing: Standards Press of China, 2000.
[27] Fichtner A, von Oheimb G, Härdtle W, et al. Effects of anthropogenic disturbances on soil microbial communities in oak forests persist for more than 100 years[J]. Soil Biology & Biochemistry, 2014, 70: 79−87.
[28] Kourtev P S, Ehrenfeld J G, Häggblom M. Exotic plant species alter the microbial community structure and function in the soil[J]. Ecology, 2002, 83: 3152−3166. doi: 10.1890/0012-9658(2002)083[3152:EPSATM]2.0.CO;2
[29] Bossio D A, Fleck J A, Scow K M, et al. Alteration of soil microbial communities and water quality in restored wetlands[J]. Soil Biology & Biochemistry, 2006, 38: 1223−1233.
[30] Gavazov K, Ingrisch J, Hasibeder R, et al. Winter ecology of a subalpine grassland: effects of snow removal on soil respiration, microbial structure and function[J]. Science of the Total Environment, 2017, 590–591: 316−324.
[31] Myers R T, Zak D R, White D C, et al. Landscape-level patterns of microbial community composition and substrate use in upland forest ecosystems[J]. Soil Science Society of America Journal, 2001, 65: 359−367. doi: 10.2136/sssaj2001.652359x
[32] Brockett B F T, Prescott C E, Grayston S J. Soil moisture is the major factor influencing microbial community structure and enzyme activities across seven biogeoclimatic zones in western Canada[J]. Soil Biology & Biochemistry, 2012, 44(1): 9−20.
[33] 胡方伟. 退化马尾松森林恢复过程中群落结构与土壤微生物多样性研究[D]. 合肥: 安徽农业大学, 2020. Hu F W. Research on community structure and soil microbial diversity during recovery process of degraded Masson pine (Pinus massoniana) forest[D]. Anhui: Anhui Agricultural University, 2020.
[34] Chen L L, Deng Q, Yuan Z Y, et al. Age-related C∶N∶P stoichiometry in two plantation forests in the Loess Plateau of China[J]. Ecologucal Engineering, 2018, 120: 14−22. doi: 10.1016/j.ecoleng.2018.05.021
[35] Liu Y, Fang Y, An S S. How C∶N∶P stoichiometry in soils and plants responds to succession in Robinia pseudoacacia forests on the Loess Plateau, China[J/OL]. Forest Ecology and Management, 2020, 475: 118394[2021−04−11]. https://doi.org/10.1016/j.foreco.2020.118394.
[36] Fu X, Yang F, Wang J, et al. Understory vegetation leads to changes in soil acidity and in microbial communities 27 years after reforestation[J]. Science of the Total Environment, 2015, 502: 280−286. doi: 10.1016/j.scitotenv.2014.09.018
[37] Zeng Q, Lal R, Chen Y, et al. Leaf and root ecological stoichiometry of Caragana korshinskii on the Loess Plateau of China in relation to plantation age[J/OL]. PLoS One, 2017, 12: e0168890 [2021−04−12]. https://doi.org/10.1371/journal.pone.0168890.
-
期刊类型引用(11)
1. 孙嘉雯,施秀珍,邵雅琪,冯鼎,王建青,刘宝,邹秉章,王思荣,黄志群. 亚热带天然次生林演替对土壤氮矿化的影响机制. 应用生态学报. 2025(01): 59-66 .  百度学术
百度学术
2. 李永涛,王振猛,杨庆山,张子龙,董爱新,周健,曹琪琪,张军. 黄河三角洲柽柳人工林土壤微生物群落结构及多样性分析. 中南林业科技大学学报. 2024(09): 80-93 .  百度学术
百度学术
3. 樊容源,叶绍明,吴昊,李梓华,李林欣,余春和. 不同林龄桉树人工林土壤细菌群落结构与功能多样性变化特征. 北京林业大学学报. 2024(12): 41-52 .  本站查看
本站查看
4. TONG Shan,CAO Guangchao,ZHANG Zhuo,ZHANG Jinhu,YAN Xin. Soil microbial community diversity and distribution characteristics under three vegetation types in the Qilian Mountains, China. Journal of Arid Land. 2023(03): 359-376 .  必应学术
必应学术
5. 刘泽勋,庄家尧,刘超,郑康,陈玲. 大同铅锌尾矿不同污染程度土壤细菌群落分析及生态功能特征. 环境科学. 2023(07): 4191-4200 .  百度学术
百度学术
6. 王玥. 不同林分密度对卓尼县落叶松林下植物多样性的影响. 南方农业. 2023(09): 273-275 .  百度学术
百度学术
7. 王明涛,赵玉红,苗彦军,孙磊,王向涛,包赛很那,王敬龙,雷变霞. 藏北一年生人工草地弃耕不同年限的土壤微生物群落特征研究. 中国草地学报. 2023(07): 100-109 .  百度学术
百度学术
8. 庞丹波,吴梦瑶,赵娅茹,杨娟,董立国,吴旭东,陈林,李学斌,倪细炉,李静尧,梁咏亮. 贺兰山东坡不同海拔土壤微生物群落特征及其影响因素. 应用生态学报. 2023(07): 1957-1967 .  百度学术
百度学术
9. 张胜男,高海燕,王志波,闫德仁,王春颖,唐凯,冯福应. 华北落叶松-白桦混交林土壤细菌群落结构与多样性及其影响因素. 东北林业大学学报. 2023(10): 98-105 .  百度学术
百度学术
10. 高禾苗,任爱天,张绍聪,袁龙义. 西藏高原不同树龄核桃林土壤细菌多样性及其影响因素分析. 北京林业大学学报. 2023(11): 100-109 .  本站查看
本站查看
11. 刘明慧,柳叶,任悦,高广磊,丁国栋,张英,赵珮杉,刘轩. 科尔沁沙地樟子松人工林土壤真菌共现网络及其与土壤因子的关系. 生态学报. 2023(23): 9912-9924 .  百度学术
百度学术
其他类型引用(6)



 下载:
下载: